کربن یکی از عناصر واکنشپذیر است که تعداد بسیار زیادی ترکیب شیمیایی با سایر عناصر تشکیل میهد. ترکیبات کربن موجود در جهان از فراوانترین ترکیبات شیمیایی هستند. مشتقات کربنی در زندگی انسان نقش مهمی دارند و درصد بسیار زیادی از جهان هستی را تشکیل دادهاند. این ترکیبات میتوانند به صورت ترکیبات هیدروکربنی، آلوتروپهای کربن، گاز کربن دی اکسید و … باشند. در این مطلب از مجله فرادرس میآموزیم مفهوم ترکیبات کربندار چیست و ویژگیها و انواع آنها را بررسی میکنیم.
آنچه در این مطلب میآموزید:
-
میآموزید ترکیبات کربن چیست و انواع آن کدام است.
-
با خواص عنصر کربن و آلوتروپهای آن آشنا میشوید.
-
تفاوت ترکیبات کربن سیر شده، سیر نشده و آروماتیک را یاد میگیرید.
-
با خواص ترکیبات کربن مانند قابلیت احتراق و پایداری آشنا میشوید.
-
واکنشها و روش نامگذاری ترکیبات کربن را میشناسید.
-
با شکل و کاربرد ترکیبات کربن آشنا شده و میآموزید ترکیبات کربن خطرناک کدامند.

در ابتدای این مطلب میآموزیم ترکیبات کربن چیست و خواص عنصر کربن را بررسی میکنیم. سپس با انواع ترکیبات آشنا شده و خواص ویژه این ترکیبات را معرفی میکنیم. در ادامه، با هیبریداسیون مشتقات کربن آشنا شده و مثالهایی از این ترکیبات را میآموزیم. همچنین، با واکنشهای این ترکیبات، فراوانی و شکل آنها، آشنا میشویم. در نهایت، کاربرد آنها و ترکیبات خطرناک کربن را میشناسیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل با شیمی ترکیبات کربندار آشنا شوید.
ترکیبات کربن چیست؟
کربن، ترکیبات و مولکولهای بسیار زیادی را تشکیل میدهد. تنوع و فراوانی ترکیبات کربن به دلیل ویژگیهای برجسته این عنصر است. مهمترین ویژگی این عنصر که باعث به وجود آمدن ترکیبات شیمیایی متعددی میشود، خاصیت به همپیوستن اتمهای کربن (زنجیری شدن) آنها است. این ترکیبات در دستههای معدنی و آلی و بر اساس نوع پیوند بررسی میشوند.

عمومیترین فرم مشتقات کربندار، متان با فرمول شیمیایی است. این دسته از ترکیبات که فراوانترین آنها نیز هستند، از اتصال عناصر کربن و هیدروژن تشکیل شده و هیدروکربن نام دارند. قسمت عمدهای از ترکیبات کربن از نوع آلی هستند که از ترکیب هیدروژن و کربن تشکیل شدهاند. با این وجود، تعداد زیادی از ترکیبات غیر آلی مانند کربن دی اکسید نیز وجود دارند.
انواع ترکیبات کربن
ترکیبات کربندار بر اساس تعداد پیوندهای بین اتمهای کربن به دو دسته ترکیبات سیرشده و ترکیبات سیرنشده تقسیم میشوند. همچنین در یک دسته بندی دیگر بر اساس نوع اتمهای موجود در ترکیبات میتوان آنها را به دو دسته آلی و معدنی تقسیم کرد.

انواع ترکیبات کربن بر اساس پیوند
کربن میتواند پیوندهای یگانه، دوگانه و سهگانه تشکیل دهد. ترکیباتی که در آنها تنها پیوند یگانه بین اتمهای کربن وجود دارد سیرشده هستند و تمایل کمتری به واکنشپذیری دارند. ترکیباتی که دارای پیوندهای دو یا سهگانه بین اتمهای کربن هستند، سیر نشده نام دارند و تمایل بیشتری به واکنش دادن با سایر ترکیبات را دارند.
در ادامه این ترکیبات را بررسی میکنیم.
ترکیبات کربن سیر شده
ترکیبات سیر شده ترکیباتی هستند که در آن اتمهای کربن با یک پیوند یگانه به هم متصل شدهاند. این ترکیبات میتوانند اشکال مختلفی مانند مولکولهای راست زنجیر یا حلقوی تشکیل دهند. آلکانها رایجترین نوع ترکیبات سیرشده هستد. متان یکی از مولکولهای خانواده آلکانها است که فرمول ساختاری و شکل آن به شکل زیر است.
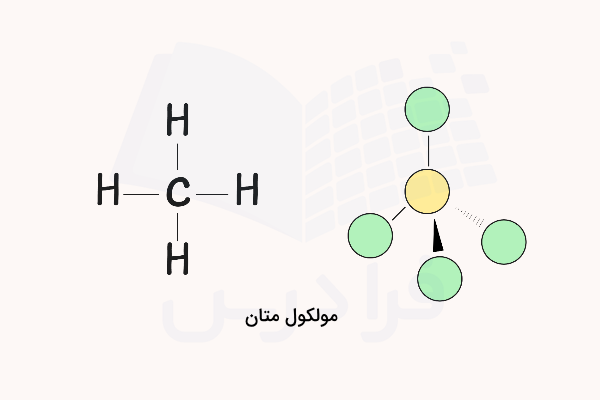
آلکان ها
سادهترین ترکیبات آلی، هیدروکربنها هستند که تنها از اتمهای کربن و هیدروژن تشکیل شدهاند. برخی از هیدروکربنها تنها پیوندهای یگانه دارند و به شکل زنجیرهای از اتمهای کربن ظاهر میشوند که به هیدروژن نیز متصلاند. این هیدروکربنها را آلکانها یا هیدروکربنهای اشباعشده مینامند.
هر آلکان دارای نام سیستماتیک مشخصی است که بر اساس تعداد اتمهای کربن تعیین میشود. نام آلکان از یک ریشه که تعداد کربنها را نشان میدهد به همراه پسوند «-ان» ساخته میشود. در ادامه برخی از آلکانها و فرمول شیمیایی آنها معرفی شده است.
| نام آلکان | فرمول شیمیایی |
| اتان | |
| متان | |
| پروپان | |
| هگزان | |
| ایزوبوتان | |
| ۲، ۴، ۴ – تری متیل پنتان | |
| دکان |
ترکیبات کربن سیر نشده
در ترکیبات سیرنشده، اتمهای کربن به وسیله پیوندهای دو گانه یا سهگانه به هم متصل شدهاند. رایجترین نوع این ترکیبات با پیوند دوگانه آلکنها و با پیوند سهگانه آلکینها هستند. در ادامه هر یک از این موارد را به اختصار توضیح میدهیم.
آلکن ها
آلکنها ترکیباتی هستند که بین حداقل ۲ اتم کربن آنها، پیوند دوگانه وجود دارد. در ننامگذاری ترکیبات آلکن، پسوند «-ِن» به انتهای نام ترکیب اضافه میشود. آلکنها میتوانند در بسیاری از واکنشهای افزایشی آلی شرکت کنند.
در تصویر زیر ساختار دو مولکول آلکن رسم شده است.
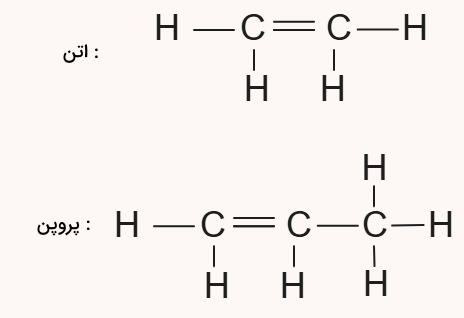
آلکین ها
آلکینها ترکیبات سیرنشدهای هستند که بین حداقل ۲ اتم کربن آنها، یک پیوند سهگانه وجود داشته باشد. نام این ترکیبات، پسوند «-ین» میگیرد و واکنشپذیر هستند. در این ترکیبات، اتمهای کربن پیوند سهگانه تنها میتوانند به یک اتم دیگر متصل شوند. بدین ترتیب، سادهترین آلکین موجود با ۲ اتم کربن و دو اتم هیدروژن اتین نام دارد و به شکل زیر است.

پیشنهاد میکنیم برای یادگیری بیشتر در مورد این ترکیبات و فرمول شیمیایی آنها، فیلم آموزش فرمول شیمیایی هیدروکربنها و نام گذاری IUPAC فرادرس که لینک ان در ادامه اورده شده است را مشاهده کنید.
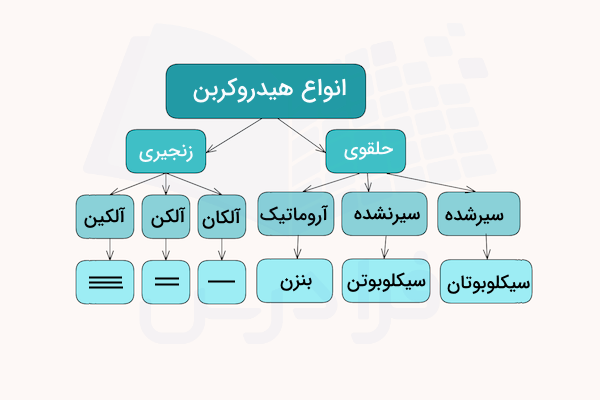
ترکیبات کربن حلقوی و آروماتیک
زنجیزههای کربنی با بیش از ۲ اتم کربن میتوانند به شکل حلقه به خود متصل شده و ترکیبات حلقوی را پدید آورند. این خاصیت مشتقات کربن باعث شده ترکیبات بسیار متنوعی به وجود آید. برای مثال بنزوییک اسید که یکی از رایجترین مواد نگهدارنده غذایی است ساختاری مانند شکل زیر دارد.
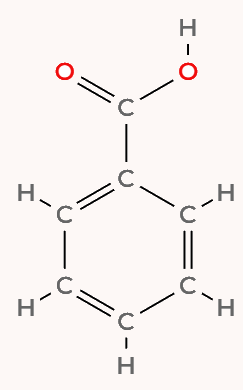
یک دسته ویژه از هیدروکربنها شامل حلقههایی از اتمهای کربن است که تقریبا همیشه ۶ اتم کربن دارند و میتوان آنها را به گونهای تصور کرد که پیوندهای یگانه و دوگانه بهصورت متناوب در حلقه قرار گرفتهاند، همانطور که در شکل زیر نشان داده شده است. به این ترکیبات، آروماتیک گفته میشود.
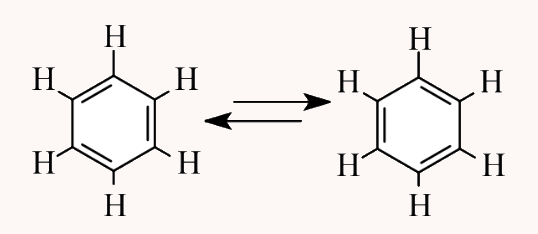
ترکیبات آروماتیک ویژگیهای خاصی دارند که به آنها آروماتیسیته (Aromaticity) گفته میشود. دو ساختار نشان داده شده در بالا، ساختارهای رزونانسی (Resonance Structures) هستند، به این معنا که اتمها در مکان خود ثابت میمانند اما پیوندهای بین اتمها میتوانند با حرکت الکترونها جابهجا شوند.
تفاوت ترکیبات سیر شده و سیر نشده
در قسمت قبل آموختیم ترکیبات کربندار سیرشده و سیرنشده چه خاصیتهایی دارند. در جدول زیر، تفاوتهای عمده این ترکیبات را توضیح دادهایم.
| ترکیبات سیرشده | ترکیبات سیرنشده |
| پیوندهای یگانه بین اتمهای کربن | پیوندهای دوگانه یا سهگانه بین کربنها |
| واکنشپذیری کمتر | واکنشپذیری بیشتر |
| واکنشهای جانشینی آلی | واکنشهای افزایشی |
| تعداد هیدروژنهای بیشتر | تعداد هیدروژنهای کمتر |
انواع ترکیبات کربن بر اساس نوع اتم ها
کربنها به دلیل ۴ ظرفیتی بودنشان میتوانند با بینهایت اتم کربن دیگر پیوند برقرار کرده و مولکولهای آلی هیدروکربنی را تشکیل دهند. همچنین، کربن میتواند با سایر اتمهای فلزی و نافلزی مانند اکسیژن گوگرد و … واکنش داده و ترکیبات معدنی را به وجود بیاورد. در ادامه این دو دسته بندی را بررسی میکنیم. همچنین، از ترکیب این دو دسته بندی، ترکیبات آلی- فلزی به وجود میآیند.
ترکیبات آلی کربنی
در ترکیبات آلی، قسمت عمده مولکول را اتمهای کربن به همراه هیدروژن تشکیل میدهند. همچنین، برخی دیگر از عناصر غیر فلزی مانند نیتروژن، اکسیژن، گوگرد و هالوژنها میتوانند به عنوان شاخه فرعی یا گروه عاملی به این ترکیبات متصل شوند. با این وجود، به دلیل کربنی بودن قسمت اصلی این مولکولها، این ترکیبات هیدروکربن یا مولکول آلی نام دارند.
از زیرمجموعه ترکیبات آلی میتوان به کربوهیدراتها، لیپیدها، پروتيینها و اسید نوکلئیکها اشاره کرد. برای مثال، ترکیباتی مانند بنزن، تولوئن، ساکاروز، هپتان و … هیدروکربن آلی هستند.
گروه عاملی
در یک زنجیره هیدروکربنی، یک یا چند اتم هیدروژن میتواند با این عناصر جایگزین شود به گونهای که ظرفیت کربن حفظ شود. این عناصر جایگزین هیدروژن، هترواتم نامیده میشوند و در گروههایی قرار دارند که خواص ویژهای به ترکیب میبخشند.
این گروهها، که به آنها گروههای عاملی میگویند، از طریق ظرفیت آزاد خود به زنجیره کربنی متصل شده و یک یا چند اتم هیدروژن را جایگزین میکنند. در جدول زیر برخی از گروههای عاملی معرفی شده است.
گروههای عاملی، خواص شیمیایی ترکیبات را مشخص میکنند. برای مثال، الکلها که شامل گروه عاملی هیدروکسیل (OH-) هستند، دارای خواص مشابهی هستند و این خواص برای الکلهایی با تعداد اتمهای کربن متفاوت، یکسان است.
طبق قرارداد، ترکیبات حاوی یونهای کربنات و بیکربنات، همچنین دی اکسید و مونوکسید کربن، به عنوان ترکیبات آلی محسوب نمیشوند، اگرچه کربن دارند.
سری همولوگ
تمام ترکیبهای آلی از زنجیرهای رو به رشد از اتمهای کربن ساخته شدهاند و بسیاری از ترکیبها دارای گروههای عاملی یکسانی هستند. چنین مجموعهای از ترکیبهای مشابه را «سری همولوگ یا همرده» (Homologous Series) مینامند. اعضای یک گروه همولوگ (همرده) از نظر ساختار شبیه یکدیگرند و ویژگیهای شیمیایی مشابهی از خود نشان میدهند. دو عضو متوالی در این سری تنها در فرمول مولکولی به اندازه یک گروه متیلن با هم تفاوت دارند.
برخی از مهمترین ویژگیهای سریهای همولوگ به شرح زیر است.
- همهی اعضا از یک فرم کلی فرمول مولکولی پیروی میکنند و گروههای عاملی یکسانی دارند.
- تفاوت هر دو عضو متوالی یک گروه متیلن است.
- تمامی اعضای این سری خواص مشابهی دارند، اما شدت واکنشها با افزایش جرم مولکولی نسبی تغییر میکند.
- خواص فیزیکی مانند حلالیت، نقطه ذوب، نقطه جوش، چگالی ویژه و … با افزایش جرم مولکولی نسبی بهتدریج تغییر میکنند.
برای مثال، در ادامه یک سری همولوگ از خانواده الکلها را معرفی کردهایم.
| نام ترکیب | فرمول شیمیایی |
| متانول | |
| اتانول | |
| پروپانول | |
| بوتانول | |
| پنتانول | |
| هگزانول |
ترکیبات معدنی کربنی
ترکیبات معدنی کربنی از پیوند شیمیایی بین تعدادی محدودی اتم کربن (نه به بزرگی هیدروکربنها) و سایر عناصر مانند اکسیژن، فلزات و …) تشکیل میشوند. ترکیبات معدنی کربن میتوانند در طبیعت یا در آزمایشگاه تشکیل شوند.
برای مثال، ترکیباتی مانند کلسیم کربنات، اکسیدهای کربن مانند کربن مونوکسید و کربن دی اکسید، اگزالاتها مانند باریم اگزالات، سولفیدهای کربن و ترکیبات کربن و نیتروژن مانند هیدروژن سیانید همگی از ترکیبات معدنی هستند. کاربیدها، کربنهالیدها و کربورانها نیز از دیگر ترکیبات معدنی کربن هستند.
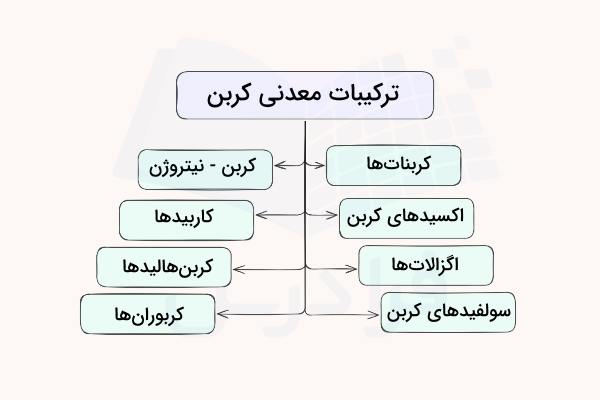
در ادامه برخی از این گروههای مولکولی را معرفی میکنیم.
- کاربیدها: کربیدها ترکیبات دوتایی هستند که از پیوند کربن با یک عنصر دیگر با الکترونگاتیویته کمتر تشکیل میشوند. نمونههایی از این ترکیبات عبارتاند از آلومینیوم کاربید، کلسیم کاربید، سیلیسیم کاربید و …
- کربن هالیدها: کربن هالیدها از اتصال عنصر کربن و هالوژنها به دست میآیند. برای مثال کربن تتراکلرید و کربن تترایدید از این موارد هستند.
- کربورانها: کربورانها مولکولهای خوشهای هستند که شامل اتمهای کربن و عنصر بور هستند. برای مثال ترکیب یک کربوران است.
ترکیبات آلی – فلزی
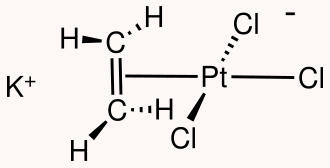
در ترکیبات آلی – فلزی، یک پیوند شیمیایی فلز – کربن در ساختار هیدروکربن وجود دارد. برای مثال، مولکول تترا اتیل سرب و نمک زایس با فرمول شیمیایی عمومی از ترکیبات آلی فلزی هستند.
آلیاژهای کربن
کربن در ترکیب بسیاری از آلیاژها نقش دارد. فولاد و چدن از شناختهشدهترین نمونهها هستند. همچنین در فرایند ذوب برخی فلزات با استفاده از کُک، مقداری کربن به ساختار آنها افزوده میشود. از میان این فلزات میتوان به آلومینیوم، کروم و روی اشاره کرد.
از دیگر آلیاژهای کربن میتوان به «اسپیگلآیزن» (Spiegeleisen) (ترکیب آهن، منگنز و کربن) و «استلایت» (Stellite) (ترکیب کبالت، کروم، تنگستن و کربن) اشاره کرد.
یادگیری شیمی یازدهم با فرادرس
برای درک بهتر شیمی ترکیبات کربن و ویژگیهای آنها نیاز است ابتدا با مفاهیمی چون عناصر جدول تناوبی، خواص فیزیکی و خواص شیمیایی، مفاهیم ترموشیمی، واکنش سوختن و پلیمرها آشنا شویم. پیشنهاد میکنیم برای یادگیری بهتر این مفاهیم به مجموعه فیلم آموزش دروس پایه یازدهم فرادرس، بخش شیمی مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مشاهده فیلمهای آموزش فرادرس که در ادامه آورده شده است، میتوانید به آموزشهای بیشتری در زمینه شیمی ترکیبات کربن دسترسی داشته باشید.
خواص عنصر کربن
عنصر کربن خواص منحصر به فردی دارد که باعث به وجود آمدن ترکیبات متنوع و متعددی از آن میشود. یکی از مهمترین این ویژگیها خاصیت به هم پیوستن اتمهای کربن است. در ادامه، مهمترین خواص عنصر کربن در تشکیل ترکیبات شیمیایی را توضیح میدهیم.
- عدد اتمی کربن ۶ و جرم اتمی آن ۱۲٫۰۱ گرم بر مول است.
- کربن اولین عضو گروه ۱۴ جدول تناوبی عناصر است.
- کربن هفدهمین عنصر فراوان زمین است و میتواند به فرم آزاد یا در ترکیبات شیمیایی وجود داشته باشد.
- عناصر کربن میتوانند به شکل زنجیرههای طولانی کربنی به هم متصل شوند.
- عنصر کربن میتواند با یک اتم کربن دیگر یا با سایر اتمها (مانند اکسیژن و نیتروژن) پیوندهای دوگانه و سهگانه با فرم پای تشکیل دهد.
- کربن به دلیل تشکیل زنجیره و پیوندهای سیر نشده به فرم آلوتروپهای گوناگونی وجود دارد.
- کربن میتواند ۴ پیوند شیمیایی تشکیل دهد و به آرایش پایدار گاز نجیب برسد. این ساختار چهارتایی میتواند تا بینهایت اتم کربن ادامه پیدا کند بدون اینکه مشکلی در پایداری پیوندها به وجود آورد.
- پیوندهای کربن با اکثر عناصر دیگر بسیار قوی هستند زیرا اندازه کوچک کربن باعث میشود هسته بتواند جفتهای الکترون اشتراکی را محکم نگه دارد، در حالی که عناصر بزرگتر پیوندهای ضعیفتری ایجاد میکنند.
- کربن چهارظرفیتی است، اما رادیکالهای آزاد کربن و کاربنها بهصورت حدواسطهای ناپایدار پدید میآیند. یونهای کربن شامل کربوکاتیونها و کربانیونها نیز عمر کوتاهی دارند.
پیوندهای شیمیایی کربن
کربن عموما با سایر اتمها پیوند کووالانسی تشکیل میدهد. این پیوندها میتواند کووالانسی قطبی یا ناقطبی باشد. از اتصال کربن با کربن پیوند کووالانسی ناقطبی و از اتصال کربن با نافلزات و فلزات پیوند کووالانسی قطبی به وجود میآید.
در برخی از موارد کربن میتواند پیوند یونی نیز تشکیل دهد. یکی از مثالهای این نوع پیوند، پیوند کربن و کلسیم در مولکول کلسیم کاربید () است. اتم کربن معمولا ۴ پیوند تشکیل میدهد اما در مواردی خاص، حالات اکسایش ۳+ تا ۳- نیز برای این اتم دیده شده است. این اتم حتی در ترکیباتی مانند هگزامتیل بنزن میتواند تا ۶ پیوند نیز تشکیل دهد.

آلوتروپهای کربن
آلوتروپ به فرمهای مختلف یک عنصر گفته میشود که خواص فیزیکی متفاوتی دارند اما خواص شیمیایی آنها مشابه است. عنصر کربن آلوتروپهای متفاوتی از جمله الماس، گرافیت، گرافن، فولرن C60، نانولولههای کربنی و … را دارد. این ترکیبات خواص فیزیکی و ظاهری متفاوتی دارند اما همگی از عناصر کربن تشکیل شده و خواص شیمیایی یکسانی دارند.
در ادامه ساختار آلوتروپهای کربن را بررسی میکنیم.
الماس
الماس یکی از آلوتروپهای شناخته شده کربن است که ساختار شبکهای سه بعدی چهاروجهی دارد. این آلوتروپ سختی فوقالعاده زیاد و هدایت گرمایی بسیار بالایی دارد. الماس ظاهری شفاف و درخشان دارد و ساختار اتمهای کربن در آلوتروپ الماس به شکل زیر است.
گرافیت
گرافیت ساختاری لایهای و دو بعدی دارد. این آلوتروپ از لایههای کربنی شش ضلعی تشکیل شده که به راحتی روی هم میلغزند و از آن در ساخت قسمت سیاه مداد استفاده میشود. گرافیت سیاهرنگ و نرم است و هادی خوبی برای گرما و الکتریسیته است. ساختار مولکولی گرافیت به شکل زیر است.
گرافن
گرافن یکی از آلوتروپهای کربن است که تنها از یک لایه کربنهای به هم متصل شش ضلعی، به شکل کندوی عسل تشکیل شده است. گرافن خاصیت انتقال الکترون بالایی دارد و مانند گرافیت، هادی گرما و الکتریسیته است. در هر حلقه ساختار گرافن، دو پیوند دوگانه بین اتمهای کربن وجود دارد.
ساختار گرافن مانند شکل زیر است.
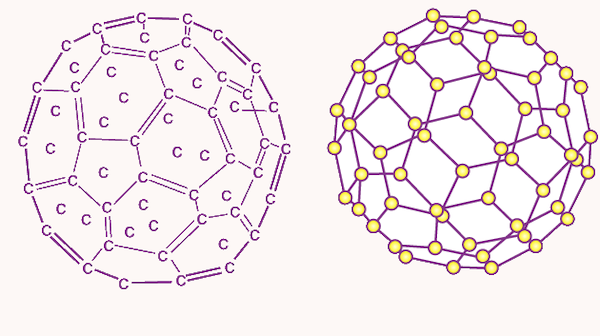
فولرن C60
فولرن C60 یکی از آلوتروپهای کربن است که در آن اتمهای کربن با تشکیل پیوندهای یگانه و دوگانه، ساختاری توپ مانند را تشکیل میدهند. در این ساختار، اتمهای کربن حلقههای پنج و شش ضلعی تشکیل میدهند و ساختاری مانند شکل زیر دارند.
نانو لولههای کربنی تک دیواره
نانو لولههای کربنی تک دیواره ساختاری بین گرافنهای تک لایه و ساختار پنج و شش ضلعی فولرن دارند.
ساختار این آلوتروپ کربن مانند شکل زیر است.

از دیگر آلوتروپهای کربن میتوان به گرافنیلن، دیامان، کربن آمورفوس، نانو فوم کربنی، کربن شیشهای، لونزدالیت (کربن شش ضلعی)، سیکلو کربن، کربن استیلنی خطی و کربن دو اتمی اشاره کرد.
واسطه کربنی
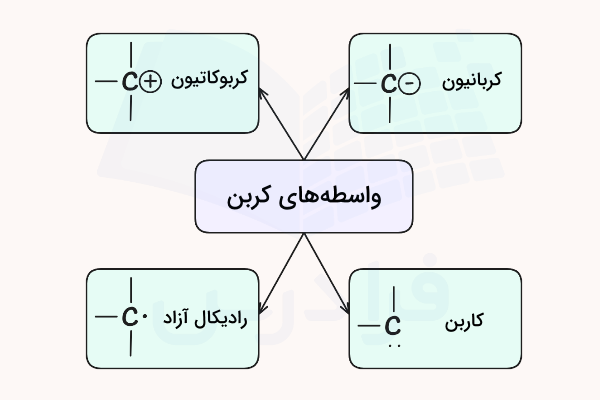
در شیمی آلی، واسطههای کربنی گونههایی موقت هستند که در طول واکنشهای شیمیایی شکل میگیرند. این گونهها اهمیت زیادی در درک روند و مکانیزم واکنشها دارند. واسطههای کربنی شامل کربوکاتیونها، کربانیونها، رادیکالهای آزاد و کاربن هستند که هرکدام ویژگیها و پایداری خاص خود را دارند.
مطالعه نحوه شکلگیری و واکنشپذیری این واسطهها به شیمیدانها کمک میکند تا پیشبینی بهتری از نتیجه واکنشها داشته باشند و مسیرهای سنتزی جدیدی طراحی کنند. در تصویر زیر انواع واسطههای کربنی مشخص شده است.
خواص ترکیبات کربن
ترکیبات کربندار به دلیل ساختار منحصربهفرد این عنصر، ویژگیهای شیمیایی و فیزیکی متنوعی دارند. آنها در دمای معمولی پایدارند و در عین حال قابلیت احتراق بالایی دارند. این ترکیبات بهسختی در آب حل میشوند و در برخی موارد میتوانند خاصیت انفجاری از خود نشان دهند.
در ادامه، با مهمترین ویژگیهای مشترک این ترکیبات آشنا میشویم.
پایداری و واکنشپذیری در گرما
بیشتر ترکیبات کربندار در دمای معمولی واکنشپذیری کمی دارند، اما هنگام گرم شدن ممکن است بهشدت واکنش دهند. برای مثال سلولز موجود در چوب در دمای اتاق پایدار است، ولی با حرارت میسوزد.
قابلیت احتراق به عنوان سوخت
ترکیبات آلی کربن معمولا قابل احتراقاند و میتوانند بهعنوان سوخت استفاده شوند. برای مثال، قطران، مواد گیاهی، گاز طبیعی، نفت و زغالسنگ از این موارد هستند. پس از سوختن این مواد، فرآورده واکنش سوخت، عمدتا کربن عنصری است. بسیاری از ترکیبات در واکنش سوختن، انرژی زیادی را به صورت نور و گرما آزاد میکنند. همچنین، از سوختن بسیاری از این ترکیبات از جمله هیدروکربنها، کربن دی اکسید و آب تولید میشود.
سوختهایی مانند زغالسنگ و نفت حاوی مقداری نیتروژن و گوگرد هستند و احتراق آنها منجر به تشکیل اکسیدهای گوگرد و نیتروژن میشود که از آلایندههای مهم محیط زیست به شمار میروند.
انحلال پذیری کم در آب
بسیاری از ترکیبات کربن غیرقطبی هستند و در آب انحلالپذیری کمی دارند. به همین دلیل آب بهتنهایی نمیتواند روغن یا چربی که از مشتقات کربن هستند را پاک کند.
خاصیت انفجاری کربن-نیتروژن
مشتقات کربن و نیتروژن اغلب خاصیت انفجاری دارند، زیرا پیوندهای میان این اتمها ناپایدار بوده و هنگام شکستن انرژی زیادی آزاد میکنند.
بوی نامطبوع ترکیبات نیتروژنی
ترکیبات کربن و نیتروژن در حالت مایع معمولا بوی مشخص و ناخوشایندی دارند، در حالیکه در حالت جامد ممکن است بیبو باشند. یکی از مثالهای این موارد نایلون است که پیش از پلیمریزه شدن بوی تندی دارد.
هیبریداسیون ترکیبات کربن
کربن یکی از عناصر شیمیایی بسیار رایج و حیاتی است که نقش مهمی در ترکیبات آلی ایفا میکند. اتمهای کربن معمولا با ترکیب اوربیتالهای مختلف پیوند برقرار میکنند و این توانایی باعث ایجاد ساختارها و خواص متنوع میشود.
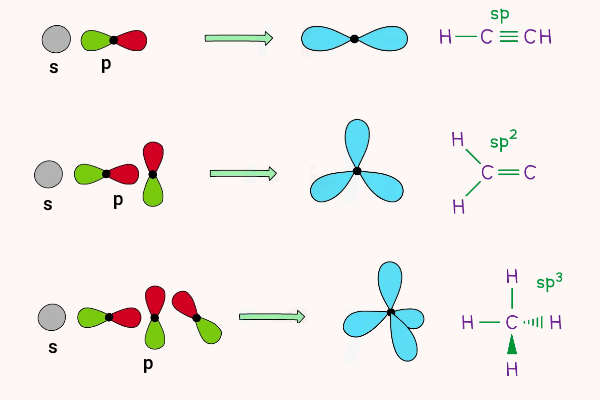
کربن میتواند سه نوع هیبریداسیون داشته باشد. این انواع هیبریداسیون ، و هستند. در بیشتر موارد، اوربیتالهای s و p در لایه دوم کربن طی هیبریداسیون با هم ترکیب میشوند. در ادامه، روش تشکیل این هیبریداسیونها را توضیح میدهیم.
- هیبریداسیون sp: یک اتم کربن به ۲ اتم دیگر به وسیله دو پیوند دوگانه یا ترکیب یک پیوند یگانه و یک پیوند سهگانه متصل میشود. زوایای پیوندی در این مورد ۱۸۰ درجه هستند.
- هیبریداسیون : یک اتم کربن به ۳ اتم دیگر به وسیله دو پیوند یگانه با اوربیتال s و یک پیوند دوگانه با اوربیتال p متصل میشود. زوایای پیوندی در این مورد ۱۲۰ درجه هستند.
- هیبریداسیون: یک اتم کربن با ۴ پیوند یگانه به ۴ اتم به وسیله یک اوربیتال s و سه اوربیتال p متصل میشود. زوایای پیوندی در این مورد ۱۰۹٫۵ درجه هستند.
مثال ترکیبات کربن
همانطور که در قسمتهای قبل توضیح داده شد، مشتقات کربندار بسیار فراوان و متنوع هستند. با این وجود میتوان خواص و انواع این ترکیبات را بر اساس نوع اتمهای شرکتکننده در این ترکیبات و نوع پیوندها مطالعه کرد. در ادامه، برخی از این ترکیبات را بررسی میکنیم.
ترکیبات کربن – هیدروژن
مشتقات کربن هیدروژن، ترکیباتی هستند که قسمت عمده آنها از اتمهای کربن و هیدروژن تشکیل شدهاند و به آنها هیدروکربن گفته میشود. ترکیبات هیدروکربن بسیار فراوان و گوناگون هستند و از خانوادههای اصلی آنها میتوان به آلکانها، آلکنها، آلکینها و ترکیبات حلقوی اشاره کرد.
ترکیبات کربن – اکسیژن
ترکیبات کربن – اکسیژن در واقع اکسیدهای کربن هستند که به آنها «اکسوکربن» نیز گفته میشود. از مهمترین مشتقات کربن-کسیژن میتوان به کربن دی اکسید اشاره کرد که یکی از مهمترین گازهای موجود و لازم برای حیات انسان و سایر موجودات زنده است. از دیگر مشتقات کربن-اکسیژن میتوان به کربن مونوکسید و کربن تری اکسید اشاره کرد.
علاوه بر اینها، چندین یون اکسیکربنی (یونهای منفی شامل فقط کربن و اکسیژن) نیز شناخته شدهاند. رایجترین آنها یون کربنات و یون اگزالات هستند. از مهمترین کربناتها، بیکربناتها و اگزالاتها میتوان به موارد زیر اشاره کرد.
- کربنات کلسیم
- کربنات پتاسیم
- کربنات منیزیم
- کربنات آمونیوم
- کربنات سدیم
- اگزالات نقره
- اگزالات باریم
- اگزالات کلسیم
- اگزالات پتاسیم
- بیکربنات آمونیوم
- بیکربنات کلسیم
- بیکربنات پتاسیم
- بیکربنات سدیم
از دیگر ترکیبات کربن-اکسیژن میتوان به کربونیلها اشاره کرد که از نوع کمپلکس بین فلز و لیگاند کربن مونوکسید تشکیل میشوند.
ترکیبات کربن – گوگرد
ترکیبات کربن گوگرد که با نام کربن-سولفید نیز شناخته میشوند، از دیگر ترکیبات فراوان کربن در زمین هستند. از این دسته از مشتقات کربنی میتوان به کربن دی سولفید، کربونیل سولفید و کربن مونوسولفید اشاره کرد.
در تصویر زیر، ساختار کربن مونوسولفید، کربن دی سولفید و کربونیل سولفید به همراه طول پیوند آنها مشخص شده است.

ترکیبات کربن – نیتروژن
نیتروژن یکی از ترکیباتی است که به راحتی با کربن پیوند شیمیایی برقرار کرده و ترکیبات مختلفی را تشکیل میدهد. از مهمترین ترکیبات کربن-نیتروژن میتوان به سیانوژن، هیدروژن سیانید و سیانوژن کلرید اشاره کرد. همچنین، گروههای مولکولی که از نیتروژن و هیدروژن تشکیل شدهاند میتوانند به شکل گروه عاملی آمین، آمید، نیتریل و … به هیدروکربنها متصل شده و ترکیبات متعددی را به وجود بیاورند.
در جدول زیر برخی از مشتقات کربن – نیتروژن به همراه شکل مولکول آنها ارائه شده است.
ترکیبات کربن – هالید
ترکیبات کربن هالید ترکیباتی هستند که از اتصال اتم کربن به اتمهای هالوژن شکیل میشود. برای مثال، ترکیب کربن تترا فلوئورید، کربن تترا کلرید و کربن تترا برمید از این ترکیبات هستند.
واکنشهای ترکیبات کربن
واکنشهای شیمیایی ترکیبات کربن به دلیل تنوع ساختار و پیوندهای مختلف این عنصر، گستره وسیعی از تغییرات شیمیایی را نشان میدهند. این واکنشها میتوانند شامل سوختن، جایگزینی، اکسیداسیون و سنتز ترکیبات جدید باشند.
در ادامه برخی از این واکنشها را بررسی میکنیم.
واکنش سوختن
واکنش سوختن مشتقات کربندار یک فرآیند شیمیایی است که در آن این ترکیبات با اکسیژن ترکیب میشوند و انرژی را به شکل گرما و نور آزاد میکنند. این واکنش معمولا دیاکسید کربن و آب تولید میکند و یکی از مهمترین منابع انرژی در زندگی روزمره است.
در ادامه، واکنش شیمیایی سوختن کربن، متان و اتانول ارائه شده است.
هیدروکربنهای اشباع شده معمولا شعلهای تمیز و بدون دود تولید میکنند، در حالی که ترکیبات غیراشباع شعلهای زرد با دود سیاه زیاد ایجاد میکنند که منجر به رسوب دوده روی سطح فلز میشود. محدود کردن جریان هوا باعث احتراق ناقص حتی در هیدروکربنهای اشباع شده و شعله دودهدار تولید میشود.
واکنش اکسیداسیون
واکنشهای اکسیداسیون در ترکیبات کربندار شامل افزودن اکسیژن به مولکولها است که در اثر آن ترکیباتی مانند الکلها به اسیدهای کربوکسیلیک تبدیل میشوند. این واکنشها با استفاده از عوامل اکسیدکنندهای مانند پرمنگنات پتاسیم قلیایی یا دیکرومات اسیدی انجام میشوند و انرژی آزاد میکنند.
برای مثال، اتانول به وسیله پتاسیم پرمنگنات یا پتاسیم دی کرومات اکسید شده و استیک اسید تولید میشود. واکنش این اکسیداسیون به شکل زیر است.
واکنش افزایشی
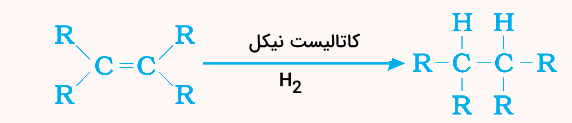
واکنش افزایشی در هیدروکربنهای غیراشباع رخ میدهد که طی آن هیدروژن به کمک کاتالیزورهایی مانند پالادیم یا نیکل به ترکیب اضافه میشود و هیدروکربنهای اشباع تولید میشوند. این واکنش معمولا در هیدروژناسیون روغنهای نباتی با استفاده از کاتالیزور نیکل به کار میرود و باعث تبدیل زنجیرههای بلند غیراشباع به زنجیرههای اشباع میشود.
در تصویر زیر، واکنش افزایشی آلکنها را مشاهده میکنید.
واکنش جانشینی
هیدروکربنهای اشباع نسبتا غیرفعال هستند و در حضور اکثر واکنشدهندهها بیاثرند. با این حال، در حضور نور خورشید، کلر میتواند به سرعت با هیدروکربنها واکنش دهد و اتمهای هیدروژن را یکییکی جایگزین کند. این واکنش، یک واکنش جانشینی نامیده میشود زیرا نوعی اتم یا گروه اتمها جایگزین اتم یا گروه دیگری میشوند.
برای مثال، واکنش کلرینه کردن متان به شکل زیر است.
فراوانی ترکیبات کربندار
ترکیبات کربندار از فراوانترین ترکیبات موجود در جهان هستی هستند. حدود ۰٫۵ درصد جرم جهان هستی از کربن تشکیل شده است. منظومه شمسی از موادی تشکیل شده است که مقدار زیادی از عنصر کربن را درون خود دارند. حدود ۰٫۰۲۵ درصد پوسته زمین از عنصر کربن تشکیل شده و یک چهارم بافتهای موجودات زنده را عنصر کربن تشکیل میدهد.
نامگذاری ترکیبات کربن
با گسترش زیاد ترکیبهای کربنی، نیاز بود که نامگذاری آنها به شکل منظمتری انجام شود. کمیتهای به نام اتحادیه بینالمللی شیمی محض و کاربردی یا «آیوپاک» (IUPAC) سیستمی ارائه داد تا ترکیبهای کربنی نام علمی و استاندارد داشته باشند. نامهای حاصل از این سیستم، در سراسر جهان استفاده میشوند و به اختصار نام IUPAC نامیده میشوند.
در این سیستم، نام ترکیبات شیمیایی کربندار به سه قسمت تقسیم میشود. این سه قست پیشوند، ریشه و پسوند نام هستند. پیشنهاد میکنیم برای درک بهتر روش نام گذاری ترکیبات هیدروکربن، مطلب نامگذاری هیدروکربنها در مجله فرادرس را مطالعه کنید.
پیشوند
پیشوند نام ترکیبات کربندار میتواند محل اتصال شاخههای فرعی، تعداد شاخههای فرعی، محل و تعداد پیوندهای دو یا سهگانه، نوع شاخه فرعی، حلقوی بودن و نوع ایزومری را مشخص کند.
محل اتصال شاخههای فرعی
محل اتصال شاخههای فرعی در هیدروکربنها، با اعدادی مشخص میشود. این اعداد، شماره کربنی هستند که شاخه فرعی به آنها متصل شده است.
تعداد شاخههای فرعی
تعداد شاخههای فرعی با عبارات مونو، دی، تری، تترا و …. مشخص میشود.
نوع شاخه فرعی
انواع مختلف گروههای مولکولی میتواند به اتمهای کربن متصل شود. برای مثال، گروههای اتیل، متیل، بوتیل، هالوژنها و … در این قسمت با نام آنها مشخص میشود.
حلقوی بودن
اگر مولکول مورد نظر، حلقوی باشد، عبارت «سیکلو» پیش از نام هسته مولکول و پس از اعداد و نام شاخههای فرعی قرار میگیرد.
پیشوند نوع ایزومر
برخی از ایزومرهای ساختاری ترکیبات کربندار با عبارات «ایزو»، «ترشیو» و … مشخص میشود. این عبارت نیز به عنوان پیشوند قبل از نام هسته یا شاخه فرعی متصل قرار میگیرد.
هسته نام
هسته نام ترکیابات کربندار، تعداد اتمهای کربن را مشخص میکند. برای مثال، آلکانهایی با نام متان، اتان و پروپان نشان دهنده وجود ۱، ۲ و ۳ اتم کربن در این ساختارها است. تعداد اتمهای کربن و نام هسته ترکیب بر اساس آنها در جدول زیر مشخص شده است.
| تعداد اتم کربن | نام هسته |
| ۱ | مت- |
| ۲ | ات- |
| ۳ | پروپ- |
| ۴ | بون- |
| ۵ | پنت- |
| ۶ | هگز- |
| ۷ | هپت- |
| ۸ | اوکت- |
| ۹ | نون- |
| ۱۰ | دک- یا دس- |
برای مثال، ترکیبی با ۹ اتم کربن و از خانواده آلکان، نونان نام دارد. ترکیبی با ۳ اتم کربن در گروه آلکین، پروپین نام دارد. الکلی با ۶ اتم کربن، هگزانول نام دارد.
پسوند
پسوند در نام ترکیبات کربندار، مشخص کننده نوع ترکیب بر اساس پیوندهای آن و گروه عاملی آن است. در ادامه نام پسوند بر اساس پیوندهای بین کربنها و گروه عاملی را معرفی میکنیم.
| نوع مولکول یا گروه عاملی | پسوند |
| آلکان | -ان |
| آلکن | -ِن |
| آلکین | -ین |
| الکل | -ول |
| آلدهید | -ال یا آلدهید |
| کربوکسیلیک اسید | -وییک اسید |
| کتون | -ون |
| آمید | -آمید |
| آمین | -آمین |
| نیتریل | -نیتریل |
| استر | -استر |
مثال نام گذاری ترکیبات کربن
برای درک بهتر موارد اشاره شده در قسمت قبل، به مثالهای زیر دقت کنید.
مثال ۱
نام ترکیبات زیر را بنویسید.
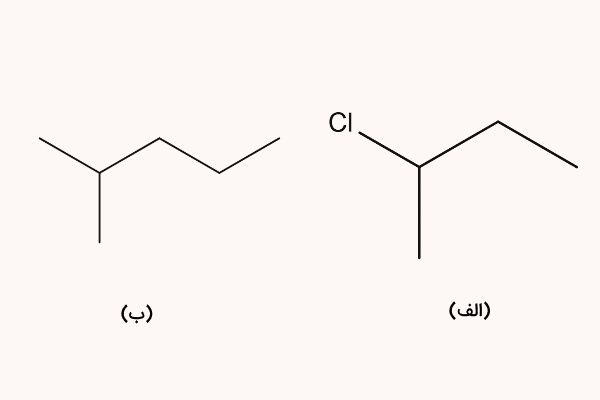
پاسخ
نام ترکیب شیمیایی الف، ۲- کلرو بوتان و نام ترکیب شیمیایی ب، ۲- متیل پنتان است. در ترکیب الف، ترکیب از ۴ اتم کربن تشکیل شده و یک آلکان راست نجیر است. شاخه فرعی روی اتم شماره ۲ قرار گرفته و نوع شاخه فرعی، هالوژن کلر است. بدین ترتیب پیشوندهای ۲ و کلرو، هسته «بوت» و پسوند «-ان» برای نامگذاری این ترکیب استفاده میشود.
به همین ترتیب ترکیب ب، شامل ۵ اتم کربن، آلکان راست زنجیر و شاخه فرعی متیل روی کربن شماره ۲ است که پیشوندهای ۲ و متیل، هسته «پنت» و پسوند «-ان» را میگیرد.
مثال ۲
نام ترکیبات زیر را بنویسید.
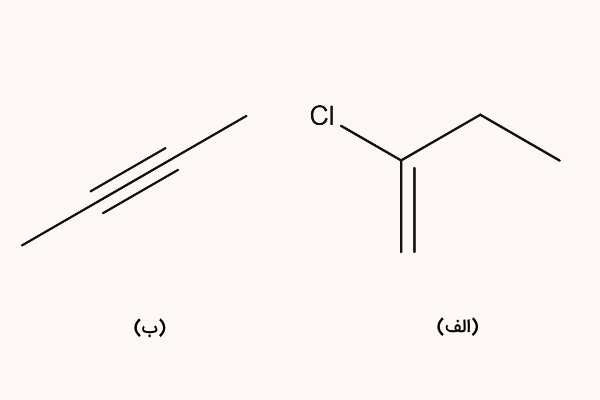
پاسخ
نام ترکیب الف، ۲ کلرو بوتن و نام ترکیب ب، ۲ بوتین است. در ترکیب الف، یک شاخه فرعی کلر روی کربن شماره ۲ قرار گرفته، ۴ اتم کربن داریم و یک پیوند دوگانه روی کربن شماره ۱ قرار دارد. بدین ترتیب پیشوندهای ۲ کلرو ، هسته «بوتن» و پسوند «-ن» برای نام گذاری این ترکیب استفاده میشود.
در ترکیب ب، ۴ اتم کربن وجود دارد که یک پیوند سهگانه روی کربن شماره ۲ قرار گرفته است. بنابراین پیشوند ۲، هسته «بوت» و پسوند «-ین» را استفاده میکنیم.
مثال ۳
نام ترکیبات زیر را بنویسید.
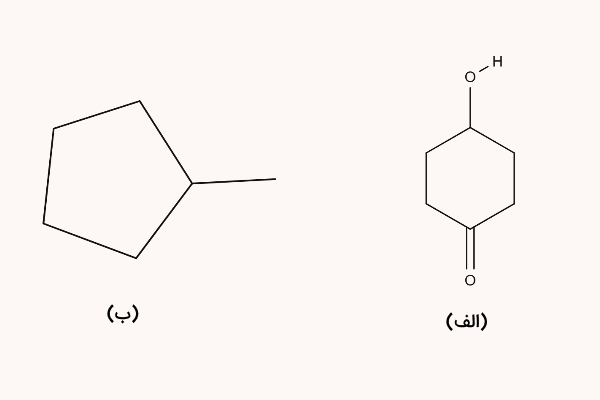
پاسخ
نام ترکیب الف، ۴- هیدروکسی سیکلوهگزانون و نام ترکیب ب، متیل سیکلوپنتان است. در ترکیب الف، یک گروه عاملی کتون و یک هیدروکسیل روی اتمهای کربن شماره ۱ و ۴ قرار دارد و نوع ترکیب آلکان حلقوی ۶ کربنه است. پس برای نام گذاری این ترکیب از پیشوندهای ۴، هیدروکسی و سیکلو، هسته «هگزن» و پسوند «-ون» استفاده میشود.
ترکیب ب، یک آلکان حلقوی با ۵ اتم کربن و یک گروه متیل روی کربن شماره ۱ است. پس نام آن از پیشوند متیل، هسته «پنت» و پسوند «-ان» تشکیل شده است.
شکلهای ترکیبات کربن
مشتقات کربنی معمولا به سه فرم وجود دارند. این فرمها ترکیبات راست زنجیر، شاخهای و حلقوی هستند. در ادامه هریک از این اشکال را توضیح میدهیم.
ترکیبات راست زنجیر
در ترکیبات راست زنجیر، اتمهای کربن به شکل یک خط مستقیم با یکدیگر پیوند برقرار کرده و قسمت عمده مولکول را تشکیل میدهند. ترکیبات راست زنجیر مانند آلکانها معمولا جرم مولکولی پایینی دارند.
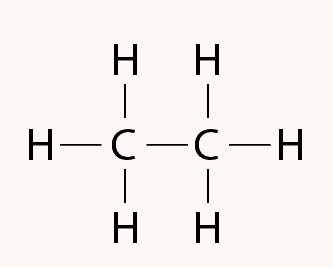
ترکیبات شاخه ای
تریبات کربنی با جرم مولکولی بالاتر معمولا به شکل شاخهای وجود دارند. در این ترکیبات برخی از اتمهای کربن با دو، سه یا چهار پیوند با اتمهای کربن دیگر برقرار میکنند. برای مثال، ایزو پنتان یکی از مثالهای این مورد است که در آن یک اتم کربن در زنجیره با ۲ اتم کربن دیگر پیوند تشکیل داده است.
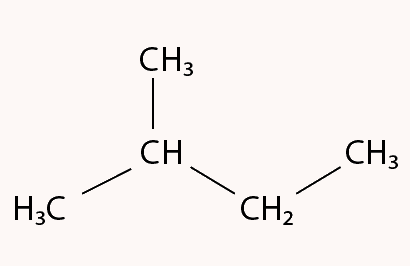
ترکیبات حلقوی
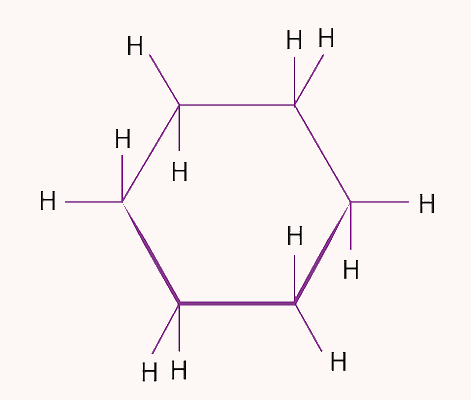
در ترکیبات حلقوی سه یا تعداد بیشتری اتم کربن به شکلی به هم متصل میشوند که یک شکل هندسی بسته را تشکیل میدهند. به این ترکیبات اصطلاحا ترکیبات «سیکلو» گفته میشود. برای مثال، سیکلوهگزان یکی از این موارد است.
کاربرد ترکیبات کربن
در این مطلب آموختیم که ترکیبات کربندار بسیار متنوع و فراوان هستند. به همین علت از این ترکیبات در صنایع و فرآیندهای گوگانون و زیادی استفاده میشود. در ادامه برخی از مهمترین کاربردهای ترکیبات را توضیح میدهیم.
سوخت و انرژی
هیدروکربنها و ترکیبات کربن-هیدروژن به عنوان سوخت برای تولید انرژی در بسیاری از فرآیندها و نیروگاهها استفاده میشوند.
تولید پلیمر
ترکیبات کربنی مانند اتیلن، پلی پروپیلن، پلی استیرن و …. در فرآیندهای پلیمریزاسیون استفاده میشوند و میتوان از آنها پلیمرهای گوناگونی با خواص کاربردی تولید کرد.
رنگ و دارو
بسیاری از مشتقات کربندار در تولید دارو و رنگها استفاده میشوند.
ساخت و ساز و جواهر
الماس که یکی از آلوتروپهای کربن است برای برش شیشه، گرانیت و سنگ مرمر و همچنین برای تولید جواهرات استفاده میشود.
صنایع مختلف
از گرافیت در تولید الکترودها برای تولید سلولهای الکترولیتی، تولید مداد، تولید روانکنندههای ماشین و .. استفاده میشود. بسیاری از قندها از ترکیبات کربنی تولید شدهاند و بسته به ویژگیهای خود در بسیاری از صنایع استفاده میشوند.
صابون و شوینده
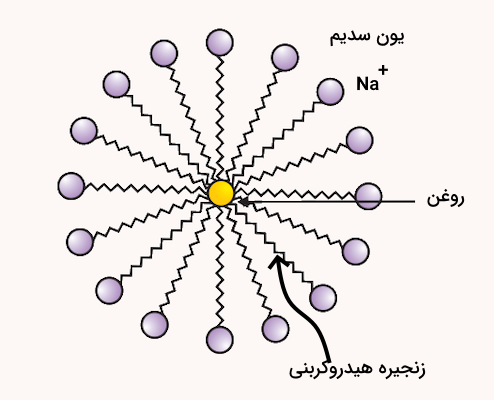
بسیاری از ترکیبات کربنی یا یک زنجیره طولانی و یک سر قطبی به عنوان صابون و شوینده استفاده میشوند. مولکولهای صابون، نمکهای سدیم یا پتاسیم اسیدهای چرب با زنجیره بلند هستند. بخش یونی صابون با آب و زنجیره کربنی آن با چربی تعامل دارد. در نتیجه، مولکولهای صابون ساختارهایی به نام میسل را تشکیل میدهند که یک سر مولکول به سمت قطره چربی و سر یونی به سمت بیرون است. این ساختار یک امولسیون در آب ایجاد میکند و به پاک شدن آلودگیها کمک میکند.
یادگیری شیمی آلی با فرادرس
برای درک بهتر واکنشها، خواص و رفتار ترکیبات کربن نیاز است ابتدا با مفاهیمی مانند انواع صورتبندی، انواع هیدروکربنها، ایزومرها، انانتیومرها، نامگذاری ترکیبات شیمی و انواع حلال آشنا شویم. پیشنهاد میکنیم برای درک بهتر این مفاهیم، به مجموعه فیلم آموزش شیمی از دروس دانشگاهی تا کاربردی فرادرس مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراجعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است میتوانید به آموزشهای بیشتری در زمینه واکنشهای مشتقات کربندار دسترسی داشته باشید.
ترکیبات کربن خطرناک
ترکیبات کربندار میتوانند در زندگی روزمره و صنایع کاربردهای فراوانی داشته باشند، اما برخی از این ترکیبات سمی و خطرناک هستند و حتی در غلظتهای کم میتوانند سلامت انسان و محیط زیست را تهدید کنند. شناخت این ترکیبات و اثرات آنها اهمیت بالایی دارد تا بتوان از مواجهه مستقیم با آنها جلوگیری کرد و ایمنی لازم را برقرار کرد.
از این مشتقات کربندار خطرناک میتوان به کربن مونوکسید، کربن دی اکسید، هیدروژن سیانید (سیانور)، کربن تترا کلرید و … اشاره کرد. در ادامه دلایل خطرناک بودن این ترکیبات را توضیح میدهیم.
- کربن مونوکسید: به راحتی وارد خون شده و به هموگلوبین متصل میشود، حتی در غلظتهای کم باعث خفگی میشود.
- کربن دی اکسید: در غلظتهای زیاد میتواند باعث خفگی شود ولی در غلظت کم تنفس را تحریک میکند.
- هیدروژن سیانید: یکی از خطرناکترین سمها برای انسان است.
- کربن تترا کلرید: این ترکیب و هیدروکربنهای کلردار میتوانند به سیستم عصبی آسیب بزنند.
به طور عمومی ترکیبهای آلی که دارای اتمهای هالوژن، گوگرد، سلنیم، تلوریم، نیتروژن، فسفر، ارسنیک، سرب و جیوه هستند، خاصیت سمی دارند.
source
