تغییرات ایجاد شده در مواد مختلف به دو گروه تقسیمبندی میشوند، «تغییرات فیزیکی» (Physical Changes) و «تغییرات شیمیایی» (Chemical Changes). اگر مادهای دچار تغییر شود اما ترکیب شیمیایی آن عوض نشود، میگوییم یک تغییر فیزیکی داشتهایم. نقطه مقابل تغییر فیزیکی، تغییر شیمیایی است که در آن یک یا چند ترکیب برای ساخت ماده جدیدی با هم مخلوط میشوند یا به مواد جدیدی شکسته میشوند. تغییر فیزیکی فقط باعث میشود خواص فیزیکی ماده عوض شوند، در نتیجه ماده جدیدی تشکیل نخواهد شد. در این مطلب از مجله فرادرس توضیح میدهیم یک تغییر فیزیکی چیست، چه ویژگیهایی دارد و چگونه میتوان آن را از تغییرات شیمیایی متمایز کرد. همچنین با ارائه چند مثال به شما کمک میکنیم تا با برخی از تغییرات فیزیکی که در اطراف شما رخ میدهند، بیشتر آشنا شوید.

تغییر فیزیکی چیست؟
خواص قابل اندازهگیری یک ماده به دو گروه خواص فیزیکی و خواص شیمیایی تقسیم میشوند. اگر تغییر اعمال شده روی ماده فقط خواص فیزیکی آن مانند حالت، اندازه، شکل، دما یا رنگ را تغییر دهد، بدون اینکه ترکیب مولکولی ماده عوض شود، پیوندی شکسته شود یا ماده جدیدی تشکیل شود، در این صورت آن تغییر را تغییر فیزیکی مینامیم. اغلب تغییرات فیزیکی موقتی و برگشتپذیر هستند، به این معنا که با معکوس کردن فرآیند میتوانیم حالت اولیه ماده را بازیابی کنیم. همچنین در یک تغییر فیزیکی جرم ماده ثابت میماند.

برای مثال تبخیر آب یک نمونه تغییر فیزیکی است. همانطور که در تصویر بالا مشاهده میکنید، با تبدیل حالت مایع به گاز یا بخار برای آب با فرمول شیمیایی H2O، تعداد، ساختار، اتمها و شکل مولکولهای آب تغییر نمیکند. فقط به علت افزایش دما و در نتیجه افزایش سرعت حرکت مولکولها، فاصله بینمولکولی زیاد میشود و تغییر حالت داریم. اگر دقت کنید، پس از این تغییر فیزیکی برخی خواص فیزیکی آب نیز علاوه بر حالت آن، تغییر میکنند. مثلا آب را میتوان مشاهده کرد، اما بخار آب قابل دیدن نیست یا کاهش چگالی آب با تبدیل شدن آن به بخار.
پس تغییرات فیزیکی شامل تغییراتی است که در حالت و دمای ماده ممکن است رخ دهند. همچنین هر نوع مخلوط شدگی مواد در شرایطی که هیچ ماده جدیدی تشکیل نشود، فرمول شیمیایی مواد تغییر نکند یا برهمکنش شیمیایی رخ ندهد، یک تغییر فیزیکی محسوب میشود. درک عمیقتر مفهوم تغییرات فیزیکی مستلزم شناخت تغییرات شیمیایی و یادگیری تفاوتهای این دو با هم است. میتوانیم بگوییم مهمترین تفاوت این دو تغییر، در اثری است که روی ترکیب ماده میگذارند.
بنابراین در ادامه ابتدا یاد میگیریم تغییر شیمیایی چیست و چه مشخصاتی دارد و سپس با جنبههای مختلف تغییرات فیزیکی بیشتر آشنا میشویم. تشخیص تغییرات فیزیکی و شیمیایی به دانشمندان کمک میکند تا بتوانند واکنشهای مختلف را پیشبینی و کنترل کنند، مواد جدید طراحی کنند و مکانیسم برخی فرآیندهای طبیعی و مهم مانند هضم غذا، فتوسنتز یا خوردگی را بهتر درک کنند.
تغییر شیمیایی چیست؟
همانطور که اشاره شد، تمام تغییراتی که در جهان اطراف ما دیده میشوند در دو گروه بزرگ تغییرات فیزیکی و تغییرات شیمیایی قرار دارند. تغییر فیزیکی فقط روی خواص فیزیکی ماده مانند رنگ، شکل، حالت و اندازه آن تاثیر میگذارد اما تغییر شیمیایی خواص شیمیایی ماده مانند فرمول یا ترکیب شیمیایی آن را عوض میکند. بنابراین در این نوع تغییر ماده اولیه از دست میرود و ماده یا مواد جدیدی ساخته میشوند. طی یک تغییر شیمیایی، خواص فیزیکی و شیمیایی مواد جدید با خواص فیزیکی و شیمیایی ماده اولیه کاملا متفاوت هستند.
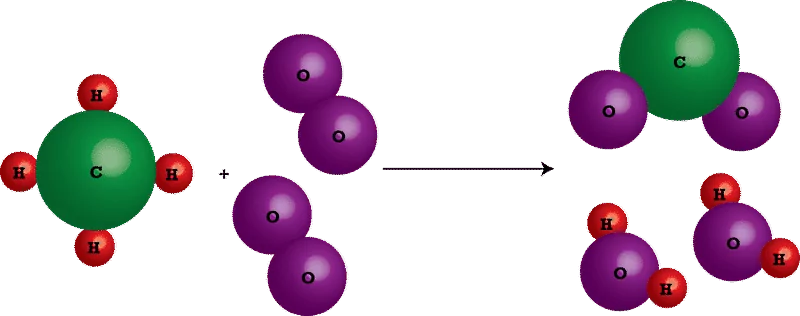
در مقایسه با شکل بخش قبل، اگر به تصویر بالا دقت کنید متوجه خواهید شد که منظور ما از تشکیل مواد جدید در یک تغییر شیمیایی چیست. واکنشدهندهها در این تغییر شامل یک مولکول متان (CH4) و دو مولکول اکسیژن (O2) هستند. اما محصولات این واکنش دو مولکول آب (H2O) و یک مولکول دیاکسید کربن (CO2) هستند. بنابراین مواد اولیه به مواد جدیدی تبدیل شدهاند که مشخصه یک تغییر شیمیایی است. یکی دیگر از مشخصات یک تغییر شیمیایی این است که معمولا همراه با جذب یا رهاسازی انرژی است. اگر طی یک تغییر شیمیایی گرما از محیط جذب شود، با یک فرآیند «گرماگیر» (Endothermic) مواجه هستیم. اما اگر طی یک تغییر شیمیایی گرما به محیط داده شود، فرآیند «گرماده» (Exothermic) داریم.
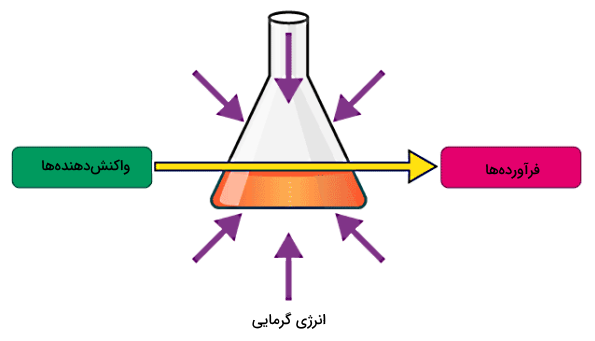
همچنین برخلاف تغییرات فیزیکی که در آنها جرم ماده ثابت میماند، در مورد یک تغییر شیمیایی جرم محصولات ممکن است با جرم واکنشدهندهها برابر نباشد، چرا که بخشی از جرم در قالب انرژی طی واکنش از دست میرود. به علاوه، معمولا یک تغییر شیمیایی تغییری گذرا یا موقتی نیست، در نتیجه اغلب نمیتوان آن را برگشتپذیر در نظر گرفت. ماهیت برگشتناپذیری تغییرات شیمیایی به شکست پیوندهای ماده اولیه و تشکیل پیوندهای جدید برای ساخت مواد جدید برمیگردد.
یادگیری انواع تغییرات در ماده با فرادرس
پیش از اینکه به ادامه مطلب بپردازیم و یاد بگیریم مشخصات یک تغییر فیزیکی چیست، در این بخش قصد داریم چند فیلم آموزشی تهیه شده در مجموعه فرادرس را به شما معرفی کنیم. مشاهده این فیلمها به شما کمک میکند تا درک بهتری نسبت به انواع خواص ماده و در نتیجه تغییراتی که در ماده رخ میدهد، بهدست آورید:
- فیلم آموزش علوم تجربی هشتم بخش شیمی فرادرس
- فیلم آموزش فیزیک دهم فرادرس
- فیلم آموزش فیزیک دهم مرور و حل تمرین فرادرس
- فیلم آموزش شیمی دبیرستان و حل تست کنکور فرادرس
- فیلم آموزش رایگان آشنایی با انواع تغییرات فیزیکی فرادرس
- فیلم آموزش رایگان آشنایی با انواع تغییرات شیمیایی فرادرس
مشخصات یک تغییر فیزیکی چیست؟
در بخش قبل یاد گرفتیم تعریف یک تغییر فیزیکی چیست و دیدیم که تغییر فیزیکی معمولا یک نوع تغییر برگشتپذیر در اندازه، رنگ، حالت یا شکل ماده است. در این بخش قصد داریم به بیان مشخصات یک تغییر فیزیکی بپردازیم تا بتوانید این تغییر را در مقایسه با یک تغییر شیمیایی بهراحتی تشخیص دهید.
پس از اینکه یک ماده دچار تغییر فیزیکی شد، نشانههایی وجود دارند که میتوانیم آنها را بهعنوان ویژگیهای یک تغییر فیزیکی در نظر بگیریم. این نشانهها عبارتاند از:
- عدم شکلگیری ماده جدید
- برگشتپذیری تغییر
- تغییر مشخصات فیزیکی ماده مانند رنگ، شکل، اندازه، دما یا حالت
- حفظ خواص شیمیایی ماده
- ثابت ماندن جرم ماده
در ادامه هر کدام از این ویژگیها را با مثال توضیح میدهیم.
عدم شکلگیری ماده جدید
میخواهیم ببینیم اولین مشخصه یک تغییر فیزیکی چیست. طی یک تغییر فیزیکی ماده جدیدی ساخته نمیشود. برای مثال تغییر فیزیکی تبدیل آب به یخ را در نظر بگیرید. در این تغییر که در واقع یکی از شش نوع تغییر حالت ماده است و انجماد نام دارد، با اینکه حالت ماده (آب) عوض میشود، اما ترکیب شیمیایی آن تغییری نمیکند. پس نمیتوانیم بگوییم ماده جدیدی ساخته شده است. ترکیب شیمیایی آب در تمام حالتهایش شامل مایع، جامد (یخ) و گاز (بخار آب) همواره بهصورت H2O است.

علت این مسئله این است که طی تغییر حالت انجماد، مولکولهای آب عوض نمیشوند، بلکه فقط فواصل و سرعت این مولکولها نسبت به هم تغییر میکند. در تصویر بالا مشخص است که مولکولهای آب با تبدیل شدن به یخ طی تغییر فیزیکی انجماد، با فواصل خیلی کمتر و در یک شبکه منظم کنار هم قرار میگیرند.
برگشتپذیری تغییر
یکی دیگر از مشخصات تغییرات فیزیکی این است که این تغییرات اغلب «برگشتپذیر» (Reversible) هستند، به این معنا که میتوانیم با معکوس کردن این فرآیند و استفاده از روشهایی مانند افزایش یا کاهش دما، مجددا ماده را به حالت اولیه آن پیش از تغییر بازگردانیم. برای مثال اگر مجددا تغییر حالت مایع به جامد در اثر انجماد را برای مادهای به نام آب در نظر بگیریم، این تغییر یک تغییر فیزیکی محسوب میشود، چون برگشتپذیر است. در واقع اگر یخ را در معرض دمای بالا قرار دهیم، به آب تبدیل میشود. بنابراین مجددا ماده به حالت اولیه خود پیش از تغییر فیزیکی انجماد بازمیگردد.

در مثال دیگر، میتوانیم یک تغییر فیزیکی دیگر برای آب به نام تبخیر را در نظر بگیریم. در این نوع تغییر حالت، ماده از حالت مایع به گاز تبدیل میشود که در مورد آب همان بخار شدن آب است. تبخیر یک تغییر فیزیکی است، چون برگشتپذیر است، به این صورت که با کاهش دمای بخار آب یا سرد کردن آن، طی تغییر فیزیکی دیگری به نام میعان به آب تبدیل میشود. پس به ماده اولیه پیش از تغییر فیزیکی دست یافتهایم.
نکته: گفتیم اغلب تغییرات فیزیکی برگشتپذیر هستند. انواع تغییر حالتهای ماده همگی جزء تغییرات فیزیکی برگشتپذیر محسوب میشوند. اما بهجز این گروه، ممکن است با برخی تغییرات فیزیکی مواجه شویم که برگشتناپذیراند.
تغییر مشخصات فیزیکی ماده
تا اینجا آموختیم پس از یک تغییر فیزیکی ماده جدیدی ساخته نمیشود و مفهوم برگشتپذیری در یک تغییر فیزیکی چیست. پیش از اینکه این بخش را ادامه دهیم، بد نیست به این نکته اشاره کنیم که فرادرس، یک دوره با عنوان «فیلم آموزشی شیمی فیزیک جامع و با مفاهیم کلیدی» تهیه کرده است که میتواند مسیر یادگیری مفاهیم شیمی فیزیک و تسلط شما بر حل مسائل مرتبط با فرمولهای آن را هموارتر کند. لینک مشاهده این فیلم آموزشی در ادامه آورده شده است:

حالا میخواهیم به آن بخش از تغییرات ماده بپردازیم که قابل دیدن هستند، مانند رنگ، شکل، اندازه. اصولا زمانی که از ویژگیهای فیزیکی یا خواص فیزیکی یک ماده صحبت میکنیم، منظورمان فرم یا شکل، اندازه، رنگ، دما و حالت آن است. برای مثال وقتی که یک کاغذ را تا میکنید یا اوریگامی میسازید، فقط شکل، فرم یا اندازه آن را تغییر دادهاید، پس یک تغییر فیزیکی روی آن اعمال شده است. قالبگیری فلزات مثال دیگری است که در آن فقط اندازه و شکل ماده تغییر میکند، بنابراین تغییر اعمال شده روی فلزات در این شرایط یک تغییر فیزیکی است.
نکته: در بررسی یک تغییر ممکن است با نشانههایی مانند تشکیل حباب حین تغییر یا شکلگیری رسوب در انتهای فرآیند نیز مواجه شویم. این موارد نشاندهنده وقوع یک تغییر شیمیایی هستند. در بخشهای بعد بیشتر با مشخصات این نوع تغییرات آشنا خواهیم شد.
حفظ خواص شیمیایی ماده
میخواهیم ببینیم ویژگی دیگر یک تغییر فیزیکی چیست. حفظ خاصیت شیمیایی ماده طی یک تغییر فیزیکی به معنای عوض نشدن فرمول شیمیایی مولکولهای سازنده ماده است. این مسئله موجب میشود که در نهایت طی تغییر فیزیکی ماده جدیدی ساخته نشود (اولین ویژگی که در مورد تغییر فیزیکی توضیح دادیم). برای مثال اگر تبدیل آب به یخ طی تغییر فیزیکی انجماد را در نظر بگیرید، در این تغییر حالت آب عوض میشود، اما مولکولهای آب تغییری نمیکنند. به عبارت دیگر، مشخصه شیمیایی محصول یک تغییر فیزیکی با مشخصه شیمیایی ماده اولیه کاملا مشابه است. از جمله مشخصات شیمیایی دیگر ماده میتوانیم به حالت اکسایش یا اشتعالپذیری آن اشاره کنیم.
ثابت ماندن جرم ماده
در یک تغییر فیزیکی اگر چه ممکن است حالت یا خواص فیزیکی ماده تغییر کند، اما جرم آن ثابت میماند. در واقع در تغییرات فیزیکی پایستگی جرم برقرار است، به این صورت که مجموع جرم مواد پیش از تغییر با مجموع جرم مواد پس از اعمال تغییر برابر است. فراموش نکنید ثابت ماندن جرم ماده طی یک تغییر فیزیکی به ثابت ماندن تعداد مولکولهای آن برمیگردد که در نتیجه ایجاد نشدن ماده جدید است.
تفاوتهای تغییر فیزیکی با تغییر شیمیایی چیست؟
پس از اینکه یاد گرفتیم مشخصات تغییر فیزیکی چیست، در این بخش تفاوتهای تغییرات فیزیکی و شیمیایی را از جنبههای مختلفی بررسی میکنیم. زمانی که با یک تغییر روبرو میشوید، اگر چهار مورد زیر را برای آن بررسی کنید، میتوانید نوع آن را تعیین کنید:
- برگشتپذیری یا برگشتناپذیری تغییر
- تغییر خواص فیزیکی یا خواص شیمیایی ماده
- تشکیل ماده جدید
- میزان جذب یا رهاسازی انرژی
در جدول زیر خلاصهای از تفاوتهای تغییرات فیزیکی و شیمیایی را مشاهده میکنید:
| علت تفاوت | تغییر فیزیکی | تغییر شیمیایی |
| تعریف | تغییر در خواص فیزیکی ماده | تغییر در خواص شیمیایی ماده |
| برگشتپذیری | اغلب برگشتپذیر و گذرا | اغلب برگشتناپذیر و دائمی |
| جذب انرژی | امکان جذب انرژی خیلی کمی وجود دارد. | در صورت جذب انرژی، واکنش گرماگیر نامیده میشود. |
| آزادسازی انرژی | هیچ انرژی آزاد نمیشود. | در صورت آزادسازی انرژی، واکنش گرماده نامیده میشود. |
| خواص | خواص شیمیایی ماده تغییری نمیکند. | خواص فیزیکی و شیمیایی ماده هر دو عوض میشوند. |
| جرم | جرم ثابت میماند. | جرم تغییری میکند. |
| اثر تغییر | تغییر خواص فیزیکی ماده مانند دما و حالت | تغییر خواص فیزیکی و شیمیایی ماده به علت تشکیل پیوندهای جدید |
| مثال | ذوب شدن یخ یا بخار شدن آب | سوختن کاغذ یا هضم غذا |
برگشتپذیری یا برگشتناپذیری تغییر
همانطور که در بخش قبل توضیح دادیم، تغییر فیزیکی یک تغییر برگشتپذیر است، به این معنا که این امکان وجود دارد ماده را با روشهایی به حالت اولیه خود قبل از اعمال تغییر فیزیکی، بازگردانیم. به همین دلیل است که تغییرات فیزیکی را تغییراتی گذرا یا موقتی در نظر میگیریم، چون ممکن است بلافاصله یک تغییر فیزیکی دیگر در جهت معکوس رخ دهد و ماده به حالت اولیه خود برگردد. نکته مهم در این زمینه این است که انرژی لازم برای ایجاد یک تغییر فیزیکی کاملا با انرژی لازم جهت معکوس کردن آن فرآیند باید برابر باشد.

در مقابل، تغییر شیمیایی زمانی رخ میدهد که مادهای با ماده دیگر برهمکنش کند و ماده جدیدی ساخته شود. این فرآیند «سنتز شیمیایی» (Chemical Synthesis) نامیده میشود. همچنین زمانی که مادهای به دو یا چند ماده مختلف و جدید شکسته شود، باز هم با تغییر شیمیایی مواجه هستیم. هر دوی این فرآیندها برهمکنش شیمیایی نام دارند و عموما «برگشتناپذیر» (Irreversible) هستند. بنابراین پس از اینکه تغییر شیمیایی برای یک ماده رخ داد، احتمال بازیابی ماده اولیه کم است.
تغییر خواص فیزیکی یا خواص شیمیایی ماده
برای اینکه درک عمیقتری نسبت به تغییرات فیزیکی و شیمیایی داشته باشیم، اولین قدم این است که ببینیم این تغییرات دقیقا روی چه بخشی از ماده اثر میگذارند. تغییرات فیزیکی ویژگیهای فیزیکی و تغییرات شیمیایی هر دو خواص شیمیایی و فیزیکی ماده را نشانه میگیرند. پس بهتر است ابتدا بدانیم کدام ویژگیهای ماده فیزیکی و کدام شیمیایی محسوب میشوند. چند نمونه از خواص فیزیکی ماده عبارتاند از رنگ، شکل، اندازه، انعطافپذیری و چگالی. در بخشهای بعد خواص فیزیکی بیشتری را معرفی خواهیم کرد.
تشکیل ماده جدید
در یک تغییر فیزیکی ممکن است مولکولهای ماده مجددا چیدمان شوند و فواصل آنها نسبت به هم عوض شود یا در ساختار چگالتری کنار هم قرار بگیرند، اما در نهایت این مولکولها عوض نمیشوند. در مقابل برای یک تغییر شیمیایی ساختار مولکولی ماده کاملا تغییر میکند. تغییر مولکولها باعث می شود دیگر ماده اولیه را نداشته باشیم و این نشاندهنده این است که ترکیبات جدیدی ساخته شدهاند.
میزان جذب یا رهاسازی انرژی
معمولا برای اینکه یک تغییر فیزیکی انجام شود، به جذب انرژی خیلی بالایی نیاز نیست. در مقابل برای انجام یک تغییر شیمیایی ممکن است مقدار خیلی زیادی انرژی جذب شود. از نظر رهاسازی انرژی نیز، در تغییرات فیزیکی عموما انرژی آزاد نمیشود، در حالی که ممکن است تغییر شیمیایی با آزادسازی انرژی بالایی همراه باشد. پس در صورتی که انرژی زیادی از محیط جذب شد یا انرژی خیلی زیادی به محیط اضافه شد، میتوانیم احتمال شیمیایی بودن تغییر را در نظر بگیریم.
چند نمونه مثال از تغییرات فیزیکی
در این بخش با بررسی چند مثال بهتر متوجه خواهید شد که یک تغییر فیزیکی چیست. میدانیم هر مادهای بسته به شرایط دمایی و فشار، در یکی از سه حالت جامد، مایع یا گاز قرار دارد. با تغییر این شرایط، مثلا با افزایش یا کاهش دما، ممکن است حالت ماده عوض شود. به این ترتیب شش نوع تغییر حالت خواهیم داشت که در جدول زیر بهطور خلاصه معرفی شدهاند:
| نام تغییر حالت | حالت اولیه ماده | حالت نهایی ماده |
| انجماد | مایع | جامد |
| ذوب | جامد | مایع |
| تبخیر | مایع | گاز |
| میعان | گاز | مایع |
| تصعید | جامد | گاز |
| چگالش | گاز | جامد |
اگر به مثالهای ارائه شده در بخشهای بعد دقت کنید، متوجه خواهید شد که شش تغییر حالت ماده جزء تغییرات فیزیکی محسوب میشوند. در ادامه توضیح بیشتری میدهیم که چرا هر کدام از این تغییر حالتها یک تغییر فیزیکی به شمار میروند. همچنین با برخی مثالهای مرسوم اطراف خود بهعنوان یک تغییر فیزیکی نیز آشنا میشویم.
تغییر حالت انجماد
به عنوان اولین مثال از یک تغییر فیزیکی، به بررسی تغییر حالت «انجماد» (Freezing) میپردازیم. در انجماد حالت ماده از مایع به جامد عوض میشود و این تغییر حالت یک تغییر فیزیکی است. میخواهیم مشخصات یک تغییر فیزیکی را برای انجماد بررسی کنیم:
- در انجماد ماده جدیدی تشکیل نمیشود.
- انجماد یک تغییر برگشتپذیر است.
- در انجماد حالت ماده عوض میشود.
- در انجماد فرمول شیمیایی ماده تغییر نمیکند.

بنابراین تمام نشانههای تغییر فیزیکی برای انجماد برقرار است. در حقیقت، وقتی که مادهای منجمد میشود، فرمول شیمیایی مولکولهای سازنده آن تغییر نمیکند، فقط چینش این مولکولها در کنار هم عوض میشود، به این صورت که مولکولها به شکل فشردهتر یا چگالتری در کنار هم قرار میگیرند. بنابراین ماده دیگر در حالت مایع نیست، بلکه وارد حالت جامد خود شده است. در واقع نام دیگر انجماد همان «بلورین شدن یا تبلور» (Crystallization) است. در این فرآیند نحوه قرارگیری اتمها و مولکولهای ماده تغییر میکند، اما مشخصه شیمیایی و ترکیب ماده دست نخورده باقی میماند.
برای مثال یخ زدن آب را در نظر بگیرید. در این مثال یخ تشکیل میشود، اما یخ در مقایسه با آب یک ماده جدید محسوب نمیشود، چون فرمول شیمیایی یخ و آب مشابه هم است. ضمن اینکه فرآیند یخ زدن آب یک فرآیند برگشتپذیر است. اگر یخ را از فریزر خارج کنیم و به عبارتی آن را در معرض گرما قرار دهیم، با جذب گرما تبدیل به ماده اولیه این تغییر فیزیکی یعنی آب خواهد شد. بنابراین انجماد آب مشخصات یک تغییر فیزیکی را دارد.
تغییر حالت ذوب
در این بخش میآموزیم فرآیند «ذوب شدن» (Melting) ماده بهعنوان دومین مثال ما از یک تغییر فیزیکی چیست و چگونه تعریف میشود. در فرآیند ذوب، حالت ماده از جامد به مایع عوض میشود. میدانیم مولکولهای یک ماده در حالت جامد با فواصل خیلی کمی در کنار هم چیده شدهاند، طوری که معمولا با یک شبکه منظم یا کریستالی مواجه هستیم. (ذرات آبی رنگ در شکل زیر).

پس نیروهای بین مولکولی در یک جامد قوی است و مولکولهای آن تقریبا هیچ گونه آزادی عملی برای حرکت در داخل ماده ندارند، بلکه فقط در جای خود بهصورت نوسانی حرکت میکنند. با افزایش دما، ممکن است سرعت حرکت این مولکولها زیاد شود. در نتیجه میتوانند حرکت بیشتری داشته باشند و در فواصل دورتری از هم قرار بگیرند. در چنین شرایطی ماده از حالت جامد خود خارج شده و به مایع تبدیل شده است. با در نظر گرفتن ویژگیهای تغییر فیزیکی بهصورت زیر، میتوانیم نتیجه بگیریم که ذوب هم مانند انجماد یک تغییر فیزیکی محسوب میشود:
- حاصل فرآیند ذوب شدن یک ماده، شکلگیری ماده جدیدی نیست.
- ذوب یک تغییر برگشتپذیر است.
- در ذوب شدن حالت ماده عوض میشود.
- پس از ذوب شدن یک ماده، فرمول شیمیایی آن تغییری نمیکند.

برای نمونه ذوب شدن یخ را در نظر بگیرید. در این تغییر فیزیکی با دریافت گرما یا خارج کردن یخ از فریزر، یخ به آب تبدیل میشود. بنابراین با اینکه حالت ماده تغییر کرده است، اما فرمول شیمیایی آن یعنی H2O عوض نمیشود. پس هیچ ماده جدیدی ساخته نشده است. همچنین این تغییر برگشتپذیر است، به این صورت که اگر آب را با قرار دادن در فریزر سرد کنیم یا از آن گرما بگیریم، مجددا به یخ تبدیل میشود (انجماد). پس دو تغییر حالت فیزیکی ذوب و انجماد عکس هم هستند. همچنین در این تغییر جرم یخ با تبدیل شدن به آب عوض نمیشود. معادله زیر برگشتپذیر بودن این دو تغییر حالت را نشان میدهد و همانطور که مشاهده میکنید، فرمول شیمیایی آب در این تغییرات عوض نمیشود:
ذوب شدن گوگرد
یک نمونه خیلی جالب از تغییرات فیزیکی که شاید بنظر برسد با یک تغییر شیمیایی روبرو هستیم، ذوب شدن گوگرد یا Sulfur جامد و تبدیل آن به گوگرد مایع است. علت اینکه ممکن است این تغییر یک تغییر شیمیایی در نظر گرفته شود، تغییر رنگ گوگرد است. اما در این تغییر هم حالت ماده عوض میشود و هم رنگ آن، در حالی که ترکیب شیمیایی ماده تغییری نمیکند.

برای نافلزهای مختلفی مانند اکسیژن و «رادون» (Radon) چنین پدیدهای رخ میدهد، یعنی تغییر حالت در این مواد نیز با تغییر رنگ ماده همراه است که نباید این نشانه را بهعنوان شیمیایی بودن تغییر آنها در نظر بگیریم.
تغییر حالت تبخیر
تا اینجا یاد گرفتیم دو مثال مهم برای یک تغییر فیزیکی چیست. فرآیند «تبخیر» (Evaporation)، سومین مثال تغییر فیزیکی و یکی دیگر از انواع تغییر حالتهای ماده است. در تبخیر حالت ماده از مایع به گاز تغییر میکند. برای اینکه بتوانیم درک بهتری نسبت به تبخیر داشته باشیم، لازم است ویژگیهای ماده در دو حالت مایع و گاز را بدانیم.
مولکولهای یک ماده در حالت مایع آزادانه روی هم میلغزند و به همین دلیل است که مایعات شکل ظرفی که در آن ریخته میشوند را به خود میگیرند. اما در حالت گازی، آزادی عمل مولکولها از این هم بیشتر است. مولکولهای یک گاز تمام ظرف یا محفظهای که در آن قرار دارند را پر میکنند. بنابراین اگر سرعت و فواصل بینمولکولی در یک مایع از حد مشخصی بیشتر شود، ماده دیگر در حالت مایع خود نیست، بلکه به حالت گازی خود تبدیل شده است.
یک نمونه مثال آشنا برای تبخیر، جوش آمدن آب است. زمانی که آب آنقدر گرم شود که به نزدیکی نقطه جوش خود یعنی دمای ۱۰۰ C برسد، در این صورت میگوییم آب جوش آمده است. جوش آمدن آب به معنای تبدیل شدن آب از حالت مایع به حالت گاز یا بخار است. در این فرآیند هیچ ماده جدیدی تشکیل نمیشود و میتوانیم با سرد کردن بخار حاصل شده، مجددا آب یا ماده اولیه در این تغییر را بازیابی کنیم. بنابراین جوش آمدن آب نمونه یک تغییر فیزیکی است:
تغییر حالت میعان
پس از اینکه یاد گرفتیم ویژگیهای تبخیر بهعنوان یک تغییر فیزیکی چیست، در این قسمت با فرآیند عکس تبخیر، یعنی «میعان» (Condensation) آشنا میشویم. در بخش قبل گفتیم که تبخیر یک تغییر فیزیکی است، پس برگشتپذیر است. برگشتپذیری تبخیر به معنای تبدیل شدن حالت گازی ماده به حالت مایع آن است که میعان نام دارد. در میعان یک ماده، فرمول شیمیایی تغییری نمیکند، ماده جدیدی ساخته نمیشود و فقط حالت ماده عوض خواهد شد.

برای مثال تشکیل قطرات آب روی شیشه پنجره در یک روز سرد و بارانی را در نظر بگیرید. علت این پدیده میعان است. هوای گرم داخل اتاق که شامل بخار آب است، در اثر برخورد با شیشه پنجره سرد میشود. در نتیجه سرعت برخی از مولکولهای بخار آب به علت سرد شدن کاهش مییابد، طوری که به قطرات آب تبدیل میشوند.
تغییر حالت تصعید
در بخشهای قبل یاد گرفتیم چهار مثال مهم برای یک تغییر فیزیکی چیست. در این قسمت یکی دیگر از انواع تغییر حالتهای ماده را بررسی میکنیم که «تصعید» (Sublimation) نام دارد. تصعید یکی از تغییرات فیزیکی جالب محسوب میشود، از این نظر که در آن ماده بدون عبور از حالت مایع، مستقیما از جامد به گاز تبدیل میشود. با توجه به اینکه نحوه قرار گرفتن مولکولها در مایعات و گازها به هم نزدیکتر است،

انتظار داریم اگر مادهای از حالت جامد خارج شده است، ابتدا به مایع و سپس به گاز تبدیل شود. اما در تغییر حالت فیزیکی تصعید چنین اتفاقی رخ نمیدهد. برای مثال تصعید یخ یا برف که در مناطقی با دمای خیلی پایین و فشار بالا مانند قطب شمال و جنوب رخ میدهد. در این مثال یخ از حالت جامد مستقیما به بخار آب تبدیل میشود.
تغییر حالت چگالش
در نهایت آخرین تغییر حالت از ماده را در این بخش با هم بررسی میکنیم تا ببینیم ویژگیهای آن بهعنوان یک تغییر فیزیکی چیست. در بخش قبل تغییر فیزیکی تصعید را معرفی کردیم. انتطار داریم تصعید بهعنوان یک تغییر فیزیکی برگشتپذیر باشد. برگشتپذیری تصعید طی فرآیند یا تغییر فیزیکی دیگری به نام «چگالش» (Desublimation) انجام میشود. در چگالش ماده مستقیما از حالت گازی خود به حالت جامد تبدیل میشود.

مثال آشنا برای تصعید، تشکیل برفک در فریزر است. در واقع در داخل فریزر میتوانید هر دو فرآیند تصعید و چگالش را بررسی کنید که چگونه به هم تبدیل میشوند. قطعات یخ داخل فریزر با تبدیل شدن به بخار طی فرآیند تصعید کم کم کوچک میشوند. این بخار در اثر برخورد با سطح سرد المنتهای فریزر، به ذرات جامدی به نام برفک تبدیل میشود. در نتیجه فرآیندهایی که داخل فریزر برای آب اتفاق میافتد، مثال خوبی برای نشان دادن گذرا یا موقتی بودن تغییرات فیزیکی مانند تصعید و چگالش است.
اغلب مخلوطها
در این قسمت بررسی میکنیم رابطه حل کردن شکر در آب با مشخصات یک تغییر فیزیکی چیست و چگونه میتوانیم این فرآیند ساده را نوعی تغییر فیزیکی در نظر بگیریم. در علم شیمی اگر دو یا چند ماده با هم مخلوط شوند، در حالی که مشخصه شیمیایی خود را حفظ کردهاند، در این صورت میگوییم ماده مخلوط داریم. در اغلب مخلوطها تغییر رخ داده شده یک تغییر فیزیکی است. شکل زیر نشان میدهد تفاوت یک ماده مخلوط با ترکیب چیست. در مخلوط ذرات مختلف از هم جدا هستند، در حالی که در ترکیب ذرات مختلف با هم پیوند شیمیایی دارند.
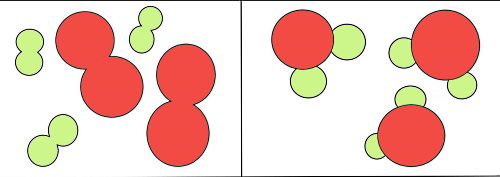
برای مثال، شاید بهنظر برسد وقتی شکر در آب حل میشوند، ماده جدیدی به نام آب قند ساخته شده است! اما این تصور اشتباه است. خواص آب و شکر پس از حل شدن در آب همچنان مانند قبل است. ترکیب شیمیایی آب دست نخورده باقی میماند، همینطور فرمول قند. بنابراین با یک تغییر فیزیکی مواجه هستیم. حتی میتوانیم آب و شکر را از هم جدا کنیم، کافی است آب را گرم کنیم تا تبخیر شود. در این صورت شکر در ته ظرف باقی خواهد ماند. در همین زمینه، میتوانید برای کسب اطلاعات بیشتر در مورد تفاوت مواد خالص و مخلوط به مطلب «مواد خالص و مخلوط چیست؟ — به زبان ساده + تعریف و مثال» از مجله فرادرس مراجعه کنید.
تبدیل شدن آلوتروپهای یک ماده به هم
«آلوتروپ یا دگرشکلی» (Allotrope) به حالتهای ساختاری مختلفی گفته میشود که یک ماده ممکن است داشته باشد. در نتیجه اگر یک آلوتروپ از مادهای به آلوتروپ دیگر آن تغییر کند، در این صورت فقط نحوه قرارگیری و چینش اتمها یا مولکولهای ماده عوض شده است و فرمول شیمیایی در این نوع تغییر عوض نمیشود. بنابراین تبدیلات آلوتروپهای یک ماده به هم نوعی تغییر فیزیکی است. برای مثال گرافیت و الماس هر دو آلوتروپهای عنصر کربن هستند که اگر به هم تبدیل شوند، نتیجه یک تغییر فیزیکی خواهد بود نه شیمیایی.
مغناطیسی شدن ماده
در این قسمت یاد میگیریم یکی دیگر از مثالهای جالب در مورد تغییر فیزیکی چیست. «مغناطیسی شدن» (Magnetization) یک ماده به معنای ایجاد و تغییر جهتگیری دو قطبیهای داخل یک ماده است. بنابراین طی این فرآیند هم ماده جدیدی ساخته نمیشود و به همین علت، برای مثال مغناطیسی شدن آهن، نمونهای از یک تغییر فیزیکی است.

از آنجا که مغناطیسی شدن ماده یک تغییر فیزیکی است، پس انتظار داریم احتمالا یک فرآیند برگشت پذیر باشد و بتوانیم با معکوس کردن آن ماده را در حالت اولیه و غیرمغناطیسیاش بازیابی کنیم. عکس فرآیند مغناطیسی شدن، دیمغناطیزیشن یا de-magnetizing نام دارد که آن هم یک تغییر فیزیکی است.
تکه کردن کاغذ یا شکستن لیوان
یک نمونه آشنا و پر تکرار از تغییرات فیزیکی فرآیندهایی مانند شکستن لیوان، تکه کردن کاغذ، بریدن یا اره کردن چوب، شکستن تخممرغ و … است. در تمام این فرآیندها فقط اندازه، شکل و فرم ماده اولیه عوض میشود، اما ترکیب شیمیایی ماده تغییری نمیکند. برای مثال زمانی که شما یک کاغذ را به چند تکه تقسیم میکنید، تکههای جدید همان فرمول شیمیایی را دارند که کاغذ اولیه دارد. فقط شکل و ابعاد آنها با کاغذ اولیه متفاوت است. حتی ممکن است بتوانیم با چسباندن تکههای کاغذ مجددا آن را به شکل و ابعاد اولیه خود بازگردانیم.
خیس یا خشک کردن لباسها
یک نمونه دیگر از تغییر فیزیکی، خیس شدن یا خشک کردن لباسها است. در این دو فرآیند ترکیب شیمیایی ماده اولیه که همان لباس است با جذب آب یا از دست دادن آب تغییری نمیکند. بنابراین چنین فرآیندهایی همگی تغییر فیزیکی محسوب میشوند. بهعلاوه با خشک شدن لباس، ماده به شکل و اندازه اولیه خود بازمیگردد و برگشتپذیری این تغییرات کاملا واضح است.
تغییرات بافت، رنگ، دما و شکل ماده
همانطور که پیشتر هم اشاره شد، هر گونه تغییری در خواص فیزیکی ماده با تغییر فیزیکی آن مرتبط است. تغییرات در بافت یا Texture ماده به تغییراتی گفته میشود که در سطح ماده ایجاد میشود و قابل دیدن است. برای مثال زمانی که یک بخش از سطح چوبی را سنباده میکشیم و سپس با واکس آن را صیقل میدهیم، یک تغییر فیزیکی روی آن انجام دادهایم. همچنین هر نوع تغییر رنگی میتواند نشاندهنده تغییر فیزیکی باشد، اما باید دقت کنید چون این عامل برای تغییرات شیمیایی هم رخ میدهد. برای نمونه رنگ کردن ماشین یک تغییر فیزیکی در نظر گرفته میشود، تا زمانی که رنگ با سطح ماشین واکنش شیمیایی ندهد.

یکی دیگر از تغییرات فیزیکی تغییرات دمای ماده است. با اینکه اثر تغییر دما را روی ماده نمیتوان دید، اما باید آن را بهعنوان یک تغییر فیزیکی در نظر بگیریم. برای مثال زمانی که یک ظرف غذا را حرارت میدهید، اثر تغییر فیزیکی افزایش دما را نمیتوانید مشاهده کنید اما با لمس ظرف، حتما متوجه آن خواهید شد. همچنین هر نوع تغییر شکل در ماده مانند چروک یا مچاله شدن لباسها یا فشار دادن یک بادکنک باد شده تغییر فیزیکی محسوب میشود.

کشیدن لاستیک
در این بخش یاد میگیریم یک مثال ساده دیگر برای تغییر فیزیکی چیست. برخی مواد مانند لاستیک را میتوانیم بکشیم، چون دارای خاصیت انعطافپذیری هستند. انعطافپذیری جزء خواص فیزیکی ماده است و هر تغییری که باعث شود این خاصیت ماده کم یا زیاد شود، یک تغییر فیزیکی محسوب میشود. برای نمونه، با کشیدن لاستیک شکل و اندازه آن تغییر میکند، اما اگر آن را رها کنیم، با حذف نیروی وارد شده مجددا به شکل و ابعاد اولیه خود برمیگردد. در این کشش هیچ ماده جدیدی ساخته نمیشود، بنابراین کشیدن لاستیک یک تغییر فیزیکی است.
خواص فیزیکی و شیمیایی چه هستند؟
در بخشهای قبل اشاره کردیم که ارتباط بین خواص مختلف ماده با یک تغییر فیزیکی چیست. اگر انواع خواص فیزیکی و شیمیایی ماده را بشناسیم، بهراحتی میتوانیم تشخیص دهیم طی یک تغییر فرضی کدام خواص از ماده عوض شدهاند و در نتیجه نوع تغییر تعیین میشود. یک خاصیت فیزیکی جنبهای از ماده است که بدون تغییر در ترکیب شیمیایی ماده قابل مشاهده یا اندازهگیری است. این گروه از خواص ماده شامل تمام خواص مکانیکی ماده و هر آنچه میشود که قابل دیدن، بوییدن، لمس کردن یا مزه کردن است.
معرفی برخی از خواص فیزیکی
خواص فیزیکی مختلفی که یک ماده میتواند داشته باشد، عبارتاند از:
- رنگ یا طولموجی از نور که توسط ماده بازتاب میشود.
- جرم
- وزن یا اثر جاذبه زمین روی جرم ماده
- دما یا میزان انرژی گرمایی یک ماده
- چگالی یا مقدار ماده در واحد حجم
- بار الکتریکی ماده
- فشار
- شکل یا فرم
- اندازه (طول)، مساحت و حجم
- نقطه ذوب، نقطه جوش و نقطه انجماد
- خاصیت بازتابندگی یا انعکاس نور یک ماده (Albedo)
- شکنندگی (Brittleness) یا تمایل به شکست در مادهای که تحت تنش قرار دارد.
- شکلپذیری (Ductility) یا آمادگی ماده برای اینکه مانند یک سیم کشیده شود.
- چکشخواری (Malleability)
- درخشش (Luster) یا میزان برهمکنش نور با سطح ماده
- حلالیت (Solubility) یا مقدار مادهای که در یک حلال حل میشود.
- چسبندگی (Viscosity) یا مقاومت ماده در مقابل تغییر شکلهای ناشی از تنش یا مقاومت ماده در مقابل جاری شدن
البته اگر بخواهیم خواص فیزیکی ماده را دقیقتر بررسی کنیم، میتوانیم این ویژگیها را از جنبههای مختلف تقسیمبندی کنیم. یکی از این دستهبندیها شامل خواص فیزیکی «گسترده» (Extensive) و خواص فیزیکی «متمرکز» (Intensive) است. خواص گسترده به اندازه یا جرمی از ماده که برای اندازهگیری انتخاب کردهاید، بستگی ندارند. برای مثال چگالی یک خاصیت فیزیکی گسترده است، به این معنا که مهم نیست چگالی یک ماده را از کدام بخش آن اندازهگیری کنید یا چه مقدار جرم برای اندازهگیری چگالی انتخاب کنید. نقطه جوش، نقطه انجماد، چسبندگی، درخشش و حالت ماده نیز جزء خواص فیزیکی گسترده بهشمار میروند. در مقابل، خواص فیزیکی متمرکز را داریم که به مقدار ماده در نمونه اندازهگیری شده بستگی دارند. برای مثال جرم، طول، حجم، مساحت و خواص ترمودینامیکی ماده مانند آنتالپی یا آنتروپی.یکی دیگر از تقسیمبندی های خواص فیزیکی بر مبنای «همسانگرد» (Isotropic) یا «ناهمسانگرد» (Anisotropic) بودن انجام میشود. خواص فیزیکی ناهمسانگرد به جهتگیری نمونه بستگی ندارند. برای مثال جرم و حجم خواص فیزیکی ناهمسانگرد محسوب میشوند. این در حالی است که خواص فیزیکی همسانگرد به جهتگیری ماده بستگی دارند. مثلا اگر به یک بلور از زاویه خاصی نگاه کنیم رنگ آن با زمانی که زاویه دید خود را تغییر دهیم، فرق میکند. بنابراین رنگ، میزان کدر بودن ماده یا Opacity در گروه خواص فیزیکی همسانگرد قرار میگیرند.
معرفی برخی از خواص شیمیایی
خاصیت شیمیایی در یک ماده تنها زمانی مشاهده میشود که مشخصه شیمیایی ماده در اثر انجام فعل و انفعالات شیمیایی عوض شود. برخی از خواص شیمیایی ماده شامل موارد زیر میشوند:
- اشتعالپذیری یا Flammability
- واکنشپذیری یا Reactivity
- حالتهای اکسایش
- میزان سمی بودن
- میزان اسیدی بودن
- PH ماده
- نیمهعمر ماده
اثر دما در ایجاد یک تغییر فیزیکی
اگر خاطرتان باشد، در بخشهای قبل توضیح دادیم که تمام تغییر حالتهای ماده نوعی تغییر فیزیکی محسوب میشوند. اما در مورد شرایط رخ دادن چنین تغییراتی زیاد توضیح ندادیم. یکی از مهمترین عوامل ایجاد کننده تغییرات فیزیکی در حالت ماده، افزایش یا کاهش دما است. در جدول زیر نشان دادهایم که کدام تغییر حالتهای فیزیکی ماده نیاز به افزایش دما و کدام نیاز به کاهش دما دارند:
| افزایش دما: عامل ایجاد تغییر حالت فیزیکی در ماده | کاهش دما: عامل ایجاد تغییر حالت فیزیکی در ماده |
| ذوب | انجماد |
| تبخیر | میعان |
نقش افزایش دما در تغییرات فیزیکی بالا، افزایش سرعت و تحرک مولکولهای ماده است، در حالی که کاهش دما موجب میشود سرعت مولکولهای ماده کم شود. فرض کنید مادهای در حالت جامد است (برای مثال یخ). در این حالت اگر دما زیاد شود، سرعت حرکت مولکولهای یخ بیشتر میشود.

بنابراین این امکان وجود دارد که مولکولها بر نیروهای قوی بینمولکولی خود غلبه کرده و در نتیجه بتوانند حرکت دوربردتری نسبت به قبل داشته باشند. با قرار گرفتن مولکولها در فواصل دورتر و ضعیفتر شدن نیروهای بینمولکولی، ماده مشخصات مایع را خواهد داشت. پس یخ به آب تبدیل شده است. این تغییر همان ذوب شدن یا اصطلاحا آب شدن یخ است.
مشخصات تغییر شیمیایی چیست؟
در این بخش توضیح میدهیم که نشانههای یک تغییر شیمیایی در مقایسه با یک تغییر فیزیکی چیست. زمانی که یک تغییر شیمیایی رخ میدهد، یک سری نشانهها به همراه دارد که عبارتاند از:
- تشکیل ماده یا مواد جدید
- تغییر رنگ
- شکلگیری گاز یا بوی خاصی
- تشکیل حباب
- تولید گرما یا نور
- ایجاد رسوب جامد از یک محلول مایع
- عدم امکان بازیابی ماده اولیه
دقت کنید تغییر رنگ ماده در اثر تغییر شیمیایی ممکن است با تغییر رنگ ماده در اثر تغییر فیزیکی اشتباه گرفته شود. در حقیقت برای تشخیص نوع تغییر در چنین مواردی که نشانهها شبیه هم هستند، باید به نشانههای دیگر توجه کنیم. در هر تغییر فیزیکی یا شیمیایی معمولا چند نشانه با هم وجود دارند و طبیعی است اگر برای تغییرات مختلف همه نشانهها یا مشخصات دیده نشوند. همچنین ممکن است تغییرات شیمیایی و فیزیکی به دنبال هم رخ دهند، طوری که تشخیص یا تفکیک آنها مشکل باشد. برای مثال جوشیدن آب را در نظر بگیرید که یک تغییر فیزیکی است و در آن آب به بخار تبدیل میشود. اگر این بخار بلافاصله به مولکولهای سازنده آن، یعنی اکسیژن و هیدروژن شکسته شود، در این صورت یک تغییر شیمیایی رخ داده است.
چند نمونه مثال از تغییرات شیمیایی
پس از اینکه با بررسی چند مثال کاملا یاد گرفتیم تغییر فیزیکی چیست، بد نیست چند نمونه مثال از تغییرات شیمیایی را نیز با هم بررسی کنیم. هضم غذا، فتوسنتز، سوختن یا احتراق هر مادهای مانند چوب یا زغال، فاسد شدن میوهها یا سبزیجات، پخت غذا و انواع خوردگیها از جمله زنگزدگی آهن از جمله مرسومترین نمونههای تغییرات شیمیایی هستند که در زندگی خود بارها با این تغییرات مواجه شدهایم.
در فاسد شدن مواد غذایی، تغییر شیمیایی باعث میشود ماده یا مواد جدیدی ساخته شوند. در نتیجه کیفیت ماده اولیه کاملا تغییر خواهد کرد و بازیابی آن امکان پذیر نیست. همچنین در فرآیند هضم نیز غذا فعل و انفعالات شیمیایی زیادی رخ میدهند که در نهایت، غذا کاملا خواص اولیه خود را از دست خواهد داد. یک نمونه از این واکنشها، تجزیه غذا به ماده جدیدی به نام گلوکز است.

برای مثال در شکل بالا، مشاهده میکنید که در سمت راست تصویر یک تغییر فیزیکی ساده به نام برش دادن یک عدد لیمو نشان داده شده است. همانطور که مشخص است، نوع ماده پیش از اعمال تغییر و پس از آن تغییری نکرده است. اما در تغییر شیمیایی سوختن چوب، پیش از واکنش، ماده واکنشدهنده چوب است اما پس از واکنش، محصول تولید شده خاکستر است. پس طی این تغییر یک ماده جدید ساخته شده است
آیا حل شدن نمک در آب یک تغییر فیزیکی است؟
یکی از بحثبرانگیزترین مباحث در زمینه تغییرات فیزیکی و شیمیایی این است که حل شدن نمک در آب چه نوع تغییری است. نمک خوراکی یا سدیم کلرید با فرمول شیمیایی NaCl یک جامد یونی است، به این معنا که پیوند شیمیایی بین یونهای سدیم و کلرید در آن از نوع پیوند یونی است. بیشتر شیمیدانها معتقداند که حل شدن یک جامد یونی مانند نمک در آب یک تغییر شیمیایی است، در حالی که حل شدن جامدات کووالانسی مانند شکر در آب تغییر فیزیکی محسوب میشود. در ادامه دو جنبه مختلف این مسئله را بررسی میکنیم تا ببینید چگونه میتوان حل شدن نمک در آب را جزء هر دو نوع تغییرات بهشمار آورد.
چرا حل شدن نمک در آب یک تغییر شیمیایی است؟
گفتیم یک تغییر شیمیایی همراه با شکلگیری ماده یا مواد جدیدی است. با حل شدن نمک در آب، یونهای کلرید و سدیم آن در آب به شکل زیر از هم جدا میشوند:
در حقیقت با حل شدن نمک در آب، پیوندهای یونی بین اتمها میشکنند و در نهایت محصولات واکنش (یونهای مثبت و منفی سدیم و کلرید و محلول در آب) با واکنشدهنده (کلرید سدیم جامد) متفاوت هستند. بنابراین مشخصات یک تغییر شیمیایی را داریم. این در حالی است که اگر یک جامد کووالانسی (جامدی که پیوند بین اتمهای سازنده آن از نوع کووالانسی است) داشتیم، در این صورت تغییر صورت گرفته فیزیکی محسوب میشد. چرا که در این حالت پیوندهای شیمیایی نمیشکنند و ماده جدیدی شکل نمیگیرد. برای مثال با حل شدن شکر در آب، مولکولهای شکر بدون هیچ تغییری در آب وجود دارند.

چرا حل شدن نمک در آب یک تغییر فیزیکی است؟
حل شدن نمک در آب را میتوان به نوعی یک تغییر فیزیکی در نظر گرفت، به این علت که هیچ تغییری در پوسته الکترونی اتمهای سدیم و کلر ایجاد نمیشود. بنابراین هیچ واکنش شیمیایی بین سدیم کلرید و حلال آب اتفاق نمیافتد. اما اگر نمک را در اسید استیک (CH3COOH) حل کنید، محصولات جدیدی به نام سدیم استات (CH3COONa) و اسید هیدروکلریک (HCl) خواهید داشت. در نتیجه این تغییر فیزیکی نیست.
گاهی اوقات علت فیزیکی در نظر گرفتن حل شدن نمک در آب را برگشتپذیری این فرآیند بیان میکنند. اگر آب را از محصول این واکنش حذف کنید، نمک بهدست خواهد آمد. اما شاید خیلی نمیتوان به این دلیل استناد کرد، چون هم یک سری تغییرات شیمیایی وجود دارند که برگشتپذیراند و هم تغییرات فیزیکی داریم که برگشتناپذیراند (مثل خورد کردن کاغذ). برای نمونه، مخلوط کردن اسید کربنیک (H2CO3) در آب یک نمونه واکنش شیمیایی برگشتپذیر محسوب میشود:
یادگیری شیمی دانشگاهی با فرادرس
آموختیم تغییر فیزیکی چست و چگونه میتوان آن را تشخیص داد. در این بخش با معرفی چند دوره به شما کمک میکنیم تا با شیمی دانشگاهی قدم به قدم آشنا شوید. مشاهده این فیلمهای آموزشی تهیه شده در مجموعه فرادرس در یادگیری بهتر انواع واکنشهای شیمیایی و در نتیجه، درک بهتر تفاوتهای تغییرات فیزیکی و شیمیایی بسیار موثر است:
- فیلم آموزش شیمی عمومی فرادرس
- فیلم آموزش شیمی عمومی ۲ فرادرس
- فیلم آموزش شیمی عمومی مرور و حل مساله فرادرس
- فیلم آموزش شیمی فیزیک فرادرس
- فیلم آموزش شیمی فیزیک حل مساله فرادرس
آزمون تغییر فیزیکی
در انتهای این مطلب از مجله فرادرس، پس از اینکه کاملا آموختید تغییر فیزیکی چیست، آزمونی متشکل از ده سوال چهار گزینهای برای شما تهیه شده است که با پاسخدهی به سوالات آن میتوانید دانش خود را در مورد تغییرات فیزیکی، مشخصات و تفاوتهای آن با تغییرات شیمیایی محک بزنید. در انتها با کلیک روی گزینه «دریافت نتیجه آزمون» نمره نهایی شما مشخص خواهد شد.
کدام یک از فرآیندهای زیر یک تغییر فیزیکی محسوب نمیشود؟
ساخت اوریگامی
مچاله کردن لباس
فقط گزینه اول یک تغییر فیزیکی نیست. یخ زدن آب همان تغییر حالت انجماد است و گفتیم تمام تغییر حالتهای ماده در گروه تغییرات فیزیکی قرار میگیرند.
در مورد ساخت اوریگامی و مچاله شدن لباس، فقط فرم، اندازه و شکل ماده اولیه تغییر کرده است. پس ماده جدیدی ساخته نمیشود و با یک تغییر فیزیکی مواجه هستیم. اما در ترش شدن شیر فعل و انفعلات شیمیایی باعث میشود ماهیت شیر کاملا عوض شود و یک تغییر شیمیایی داشته باشیم.
طی یک تغییر فیزیکی کدام مورد حتما ثابت میماند؟
گزینه اول درست است. همانطور که توضیح دادیم خواص فیزیکی ماده مانند رنگ، شکل، اندازه و حالت ماده طی تغییر فیزیکی «ممکن» است عوض شوند. برای مثال ممکن است در یک تغییر فیزیکی اصلا حالت ماده عوض نشود، مانند مورد شکستن لیوان.
همچنین ممکن است طی یک تغییر فیزیکی مانند تبخیر آب رنگ ماده تغییری نکند یا اصلا متوجه تغییر رنگ آن نشویم، اما مطمئن هستیم که حالت ماده عوض شده است. آن خاصیتی از ماده که قطعا در یک تغییر فیزیکی ثابت میماند، جرم ماده است.
کدام گزینه ممکن است در یک تغییر فیزیکی تغییر کند؟
اینکه ماده از چه ساخته شده است.
ساختار مولکولی ماده
گزینه سوم درست است. گفتیم در یک تغییر فیزیکی خواص فیزیکی ماده مانند رنگ، حالت و شکل آن ممکن است عوض شوند. یکی دیگر از این خواص فیزیکی، دمای ماده است. اما در یک تغییر فیزیکی همیشه جرم ماده ثابت میماند. همچنین ساختار مولکولی یا فرمول شیمیایی ماده فقط در تغییرات شیمیایی عوض میشوند.
کدام گزینه یک تغییر فیزیکی محسوب میشود؟
سوختن گاز متان
محلول آب و شکر
گزینه آخر تغییر فیزیکی است. تمام فرآیندهای سوختن یا احتراق در گروه تغییرات شیمیایی قرار میگیرند. همچنین فتوسنتز مانند هضم غذا یک تغییر شیمیایی است.
آیا دما روی تغییرات فیزیکی و شیمیایی موثر است؟
فقط روی تغییرات فیزیکی تاثیرگذار است.
فقط روی تغییرات شیمیایی تاثیرگذار است.
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
کدام مخلوط زیر در نتیجه یک تغییر فیزیکی نیست؟
مخلوط آب و روغن
مخلوط نمک و ماسه
مخلوط شکر و آب
مخلوط اسید و باز
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
تبخیر نیتروژن مایع یک تغییر … و مخلوط کردن جوش شیرین و سرکه یک تغییر … است.
فیزیکی – شیمیایی
شیمیایی – فیزیکی
فیزیکی – فیزیکی
شیمیایی – شیمیایی
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
تبدیل گرافیت به الماس یک تغییر … است.
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
حل شدن نمک در آب یک تغییر … است.
هم میتواند شیمیایی باشد و هم فیزیکی.
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
کدام گزینه جز خواص فیزیکی یک ماده محسوب نمیشود؟
اشتعالپذیری
مشاهده پاسخ تشریحی برخی از سوالات، نیاز به عضویت در مجله فرادرس و ورود به آن دارد.
source
