نیکل یکی از عناصر فلزی جدول تناوبی و از دسته عناصر فلزات واسطه است. این عنصر با نماد شیمیایی و عدد اتمی ۲۸ در دوره چهارم جدول تناوبی قرار گرفته است. این عنصر یکی از عناصر حیاتی برای بدن است که مصرف بیش از اندازه آن میتواند باعث آسیب به سلامت شود. در این مطلب از مجله فرادرس میآموزیم عنصر نیکل چیست و چه خواص و کاربرد و خطراتی دارد.
آنچه در این مطلب میآموزید:
-
میآموزید عنصر نیکل چیست و چه ویژگیهای فیزیکی و شیمیایی دارد.
-
یاد میگیرید نیکل چگونه تولید میشود و چه منابع و انواعی دارد.
-
با مهمترین ترکیبات و آلیاژهای نیکل و کاربردهای صنعتی آن آشنا میشوید.
-
میتوانید واکنشهای نیکل با آب، هوا، هالوژنها و اسیدهای مختلف را تشخیص دهید.
-
دلایل و کاربرد زیستی نیکل را میآموزید و با خطرات و نکات ایمنی آشنا میشوید.
-
مزایا، معایب و تاریخچه استفاده از نیکل در صنایع گوناگون را درک میکنید.



در ابتدای این مطلب میآموزیم عنصر نیکل چیست و خواص آن کدامند. سپس به بررسی روش تولید و منابع و انواع عنصر نیکل میپردازیم. در ادامه ترکیبات نیکل را میشناسیم و با آلیاژها و واکنشهای آن آشنا میشویم. در نهایت به توضیح کاربرد، خواص زیستی، نکات ایمنی و مزایا و معایب این عنصر پرداخته و تاریخچه آن را میشناسیم. با مطالعه این مطلب تا انتها میتوانید به شکلی کامل بیاموزید عنصر نیکل چیست.
عنصر نیکل چیست؟
عنصر نیکل با نامهای دیگری مانند اسمالتیت، گارنیریت، پنتلاندیت و میلریت که نام سنگهای معدنی آن است نیز شناخته میشود. نیکل بیست و دومین عنصر فراوان زمین و هفتمین عنصر فراوان بین فلزات واسطه است. در ادامه خواص این عنصر فلزی پرکاربرد را بررسی میکنیم.
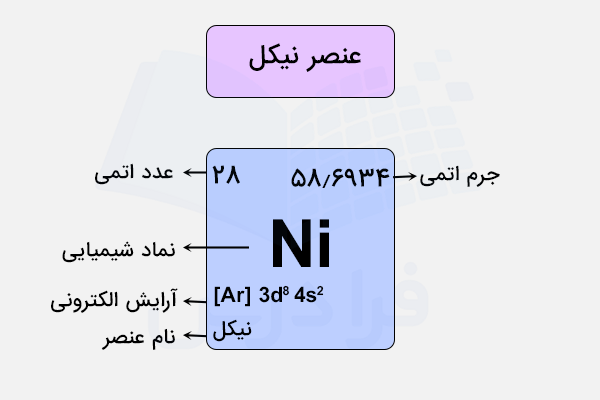
خواص فیزیکی نیکل
عنصر نیکل، عنصری با نقطه ذوب بسیار بالا، جلای فلزی و ظاهری درخشان است. این عنصر یکی از عناصر حیاتی بدن است و به دلیل خواص منحصر به فردی که دارد، در بسیاری از صنایع استفاده میشود. در ادامه برخی از خواص شیمیایی عنصر نیکل را بررسی میکنیم.
- این عنصر در دمای ۲۰ درجه سانتیگراد در حالت جامد است. نقطه ذوب عنصر نیکل ۱۴۵۵ درجه سانتیگراد است.
- نقطه جوش این عنصر برابر با ۲۹۱۳ درجه سانتیگراد است.
- دانسیته آن برابر با ۸٫۹ گرم بر سانتی متر مکعب است.
- نیکل فلزی با رنگ نقرهای – سفید و بسیار سخت است.
- این فلز چکشخوار و هادی است.
- این فلز هادی خوبی برای گرما و الکتریسیته است.
- این فلز تنها در حالت خالص جلای فلزی داشته و ظاهری آینه مانند دارد که نور را منعکس میکند.
- ترکیب نیکل و مس به جلای فلزی این ماده سایهای قرمز رنگ میدهد.
- این فلز فرومغناطیس است.

خواص شیمیایی نیکل
عنصر نیکل عنصری با نماد شیمیایی Ni در گروه دهم و دوره چهارم جدول تناوبی قرار دارد و متعلق به دسته عناصر واسطه (بلوک d) است. در ادامه میآموزیم برخی از خواص شیمیایی عنصر نیکل چیست.
- نیکل چندین ایزوتوپ دارد.
- جرم اتمی این عنصر برابر با ۵۸٫۶۹۳ است.
- ظرفیت این عنصر برابر با ۲+ است.
- این فلز در اسیدهای رقیق به آرامی حل میشود.
- این فلز پرتوزا بوده و سمی است.
- زیست سازگاری و مقاومت در برابر خوردگی در بدن
- آرایش الکترونی این فلز به شکل است.

ایزوتوپهای نیکل
نیکل طبیعی از ۵ ایزوتوپ پایدار نیکل – ۶۴ (٪۰٫۹۱)، نیکل – ۶۲ (٪۳٫۵۹)، نیکل – ۶۰ (٪۲۶٫۱۰) و نیکل – ۵۸ (٪۶۸٫۲۷) تشکیل شده است. این عنصر ساختاری مکعبی مرکز پر دارد و تنها با استفاده از واکنشهای هستهای و با بمباران ذرات پرانرژی قابل شکستن است.
یادگیری خواص نیکل با فرادرس
برای درک بهتر این موضوع که عنصر نیکل چیست، ابتدا باید با مفاهیمی چون اتمها و مولکولها، ایزوتوپها، مفهوم پیوند و کوئوردیناسیون، نیمواکنشها و پیلهای الکترولیتی و گالوانی آشنا شویم. پیشنهاد میکنیم برای آشنایی بهتر با این مسائل، به مجموعه فیلم آموزش شیمی از دروس دانشگاهی تا کاربردی فرادرس مراجعه کنید که با زبانی ساده ولی کاربردی به توضیح این مفاهیم میپردازد.
همچنین، با مراحعه به فیلمهای آموزش فرادرس که در ادامه آورده شده است میتوانید به آموزشهای بیشتری در زمینه مواد شیمیایی دسترسی داشته باشید.
تولید عنصر نیکل
عنصر نیکل با استفاده از مجموعه عملیاتهای متالورژی مانند استخراج از معادن، ذوب و پالایش میشود. این فلز در موارد نادری به شکل فلز خالص یافت میشود. بیشتر منابع فلز نیکل، نمکهای معدنی آن هستند. این ترکیبات معمولا شامل نیکل، مس و سایر مواد معدنی هستند.
استخراج نیکل از ترکیبات سنگ معدنی با استفاده از فرآیندهایی مانند خرد کردن، آسیاب کردن و جداکردن با استفاده از اختلاف چگالی است. مواد به دست امده از این فرآیندها غلظت بالایی از نمکهای نیکل دارند و با استفاده از گداختن و ذوب شدن در یک محیط کاهنده، ناخالصیها از آنها جدا شده و به نیکل مات تبدیل میشوند.
اگر تا اینجای مطلب را مطالعه کردهاید، با عنصر نیکل و خواص فیزیکی و شیمیایی آن آشنا شدهاید. در ادامه مطلب نیز به بررسی سایر نکات این عنصر میپردازیم.
پیشنهاد میکنیم برای مطالعه بیشتر این نوع مطالب و دسترسی همیشگی و رایگان به آنها در موبایل خود، اپلیکیشن رایگان مجله فرادرس را نصب کنید تا همیشه به مطالب مجله فرادرس دسترسی داشته باشید.
برای نصب اپلیکیشن رایگان مجله فرادرس، کلیک کنید.
خالص سازی پس از این مرحله با استفاده از الکترولیز یا استخراج حلال انجام میشود. نیکل به دست آمده معمولا طی یک فرآیند گداخت دیگر برای تولید آلیاژ استفاده میشود. این فلز اغلب در یک کوره قوس کربنی یا القایی (تحت خلا یا اتمسفر خنثی)، گرم میشود تا خلوص آن افزایش یابد.
منابع عنصر نیکل
مهمترین منابع نیکل شامل سنگهای معدنی مانند پنتلندیت همراه با پیروتیت نیکلدار، کالکوپیریت و لاتریتهای نیکلدار مانند گارنیرایت و سیلیکات منیزیم-نیکل با ترکیب متغیر، هستند.
متالورژی نیکل دربرخی از جزئیات پیچیده است و بسیاری از مراحل آن بسته به نوع سنگ معدنی مورد پردازش متفاوت است. بهطور کلی، سنگ معدن به دینیکل تریسولفید با حالت اکسیداسیون (۳+) تبدیل میشود، سپس در هوا حرارت داده شده و اکسید نیکل با عدد اکسایش ۲ تولید میشود. این اکسید سپس با کربن کاهش یافته و فلز نیکل بهدست میآید. بخشی از نیکل با خلوص بالا نیز از طریق فرآیند کربونیل تولید میشود.
در طبیعت، نیکل بهصورت کانیهایی ترکیبشده با آرسنیک، آنتیموان و گوگرد یافت میشود. برخی از این کانیها در ادامه معرفی شده است.
- سولفید نیکل
- آرسنید نیکل
- آنتیمونید نیکل
- دی ارسنید نیکل
- تیواس آرسنید نیکل
- تیواس آنتیمونید نیکل
انواع عنصر نیکل
علاوه بر سنگهای معدنی نیکل، این فلز به شکل ترکیب در آلیاژهای بسیار متنوعی نیز وجود دارد که معمولا برای فرآیند آبکاری نیکل انجام میشوند. در ادامه، میآموزیم مهمترین انواع فلز نیکل چیست.
سولفید ماگمایی
سولفید ماگمایی به باقیماندههای بسیار ارزشمند معدنی مافیک (دارای منیزیم و سیلیکات) و فوق مافیک سنگهای آتشفشانی گفته میشود که طی فرآیند تولید ماگمای آتشفشان تولید میشود. این باقیماندهها شامل مقادیر قابل توجهی از فزات نیکل، مس و پلاتین هستند.

با سرد شدن و کریستاله شدن مواد مذاب آتشفشان، ترکیبات معدنی سولفید با چگالی بالاتر به پایین رفته و ته نشین میشوند. این فرآیند به افزایش خلوص ترکیبات شاکل فلز با چگالی بالاتر کمک میکند. این نوع از ترکیب فلز نیکل یکی از مهمترین منابع فلزات در سراسر جهان است.
لاتریت
لاتریتها خاکها و ترکیبات سنگی هوازده هستند. این ترکیبات رنگی قهوهای یا قرمز قابل تشخیص دارند و مقادیر بسیار زیادی فلز آهن و اکسید آلومینیوم دارند. این ترکیبات معمولا در مناطق استوایی یا فوق استوایی با بارانهای فصلی سنگین و دمای بالاتر تشکیل میشوند. این ترکیبات به عنوان نتیجه یک فرآیند شیمیایی قوی هوازدگی در طی مدت زمان طولانی تشکیل میشوند.

این فرآیند، مواد معدنی موجود در لایههای بالاتر سنگها را شسته و ترکیبات غلیظتر فلزی موجود در لایههای پایینتر را غلیظتر میکند زیرا این ترکیبات معمولا چگالی بالاتری دارند.
این ترکیبات لاتریت از نظر تجاری اززش بالایی دارند زیرا شامل مقادیر قابل توجهی از فلزات با ارزش مانند نیکل و کبالت هستند.
ترکیبات نیکل
نیکل به دلیل ظرفیت دوتایی خود ترکیباتی دو ظرفیتی تشکیل میدهد. با این وجود در برخی از ترکیبات نیکل عدد اکسایش ۱- تا ۴+ برای آن مشاهده شده است. رنگ ترکیبات نیکل آبی و سبز هستند و این ترکیبات معمولا آبپوشیدهاند.
ترکیبات نیکل با حالت اکسیداسیون ۲+ کاربردهای صنعتی متنوعی دارند. بهعنوان مثال کلرید نیکل، نیترات نیکل و سولفامات نیکل در وانهای آبکاری نیکل استفاده میشوند.
سولفات نیکل علاوه بر آبکاری در تهیه کاتالیزورها، لعابهای پایه و مواد ثابتکننده برای رنگرزی و چاپ منسوجات بهکار میرود. اکسید نیکل و پراکسید نیکل برای استفاده در سلولهای سوختی و باتریهای ذخیرهای تهیه میشوند. فریتهای نیکل نیز بهعنوان هستههای مغناطیسی در تجهیزات الکتریکی مانند آنتنها و ترانسفورماتورها کاربرد دارند.
نیکل هیدروکسید
نیکل هیدروکسید با استفاده از رسوبدهی با محلولهای قلیایی با نمکهای نیکل (اا) تهیه شده و کریستالهای سبزرنگ دارد. این ترکیبات به خوبی در اسید و آمونیاک هیدروکسید حل میشود اما در آب نامحلول است.

برای درک بهتر خواص نیکل و فلزات مشابه آن و ترکیباتی که تشکل میدهند پیشنهاد میکنیم مطلب عناصر واسطه و خصوصیات آنها مجله فرادرس را مطالعه کنید.
نیکل اکسید
نیکل اکسید یک پودر سبز رنگ جامد است که با حرارت دیدن به زرد تغییر رنگ میدهد. تولید این ماده با استفاده از حرارت دادن نیکل در اکسیژن مشکل است . روش عمده تولید این ترکیب، حرارت دادن نیکل هیدروکسید، کربنات یا نیترات نیکل است. نیکل اکسید در اسید حل میشود اما در آب داغ و سرد نامحلول است.
تجزیه حرارتی ترکیبات نیکل هیدروکسید ()، نیکل کربنات () و نیکل نیترات () به تولید اکسید نیکل () منجر میشود. در ادامه خواص این ترکیب آورده شده است.
| خواص ترکیب اکسید نیکل | توضیح خواص |
| فرمول شیمیایی | |
| رنگ و حالت | پودر جامد سبزرنگ |
| حالت اکسایش |
دو ترکیب عمده اکسید نیکل، اکسید نیکل سیاه و سبز هستند. اکسید نیکل سیاه از نظر شیمیایی فعال و رنگ سبز آن بی اثر است. پیشنهاد میکنیم برای درک بهتر خواص این ترکیب، مطلب اکسید چیست مجله فرادرس را مطالعه کنید.
نیکل هالید
ترکیب نیکل با تقریبا تمامی هالوژنها وجود دارد. در این ترکیبات، یک اتم نیکل به صورت یونی با دو هالوژن ترکیب میشود. این ترکیبات معمولا رنگی بین زرد تا قهوهای تیره دارند. تولید تمامی این ترکیبات بجر نیکل فلوئورید به صورت مستقیم از عنصر خالص نیکل ممکن است.
ترکیب نیکل فلوئورید از واکنش مولکول دو اتمی فلوئور با نیکل کلرید در دمای ۳۵۰ درجه سانتیگراد انجام میشود. بیشتر ترکیبات نیکل هالید در آب محلول هستند و ترکیبات شش آبه تشکیل میدهند. تنها نیکل فلوئورید به صورت جزئی در آب حل میشود و ترکیب ۳ آبه تشکیل میدهد.
کمپلکسهای نیکل
نیکل (اا) میتواند کمپلکسهای پایدار متعددی را تولید کند. با وجود این که این عنصر حالت اکسایش دیگر بجز ۲ ندارد، میتواند کمپلکسهای بسیار زیادی را تولید کند. برای مثال، کمپلکسهایی با ساختار فضایی چهاروجهی، مربع مسطح، هرمی مربعی و دو هرمی مثلثی با لیگاند سیانید (CN) از این عنصر وجود دارد.

تصویر بالا از چپ به راست نشاندهنده رنگ کمپلکسهای و و و در آب است. عبارت «نیکل غیرعادی» (anomalous nickel) به دلیل این رفتار عنصر نیکل به آن نسبت داده شده است. در ادامه مشخصات دو کمپلکس از نیکل و سیانید ارائه شده است.
| فرمول شیمیایی | رنگ و ساختار هندسی |
| سبز و تتراهدرال | |
| قرمز و مربع مسطح |
سایر ترکیبات نیکل
بجز موارد ارائه شده، نیکل میتواند ترکیبات دیگری را نیز تشکیل دهد. برخی از این ترکیبات در آب محلول هستند و در آب ممکن است یون هیدرات نیکل (اا) تشکیل دهند. برخی دیگر از ترکیبات نیکل در آب محلول نیستند. در ادامه میآموزیم سایر ترکیبات عنصر نیکل چیست.
ترکیبات نیکل محلول در آب
ترکیباتی از نیکل که در آب به خوبی حل میشوند در ادامه نام برده شده است.
- نیکل استات
- نیکل کلرید
- نیکل یدید
- نیکل نیترات
- نیکل سولفات
ترکیبات نیکل نامحلول در آب
ترکیباتی از نیکل که نمیتوان آنها را در آب حل کرد در ادامه معرفی شده است.
- نیکل اکسید
- هیدروکسیدهای نیکل
- سولفید نیکل
- نیکل آرسنید
- نیکل کرومات
- نیکل کربنات
- نیکل فسفات
- نیکل سلنید
آلیاژهای نیکل
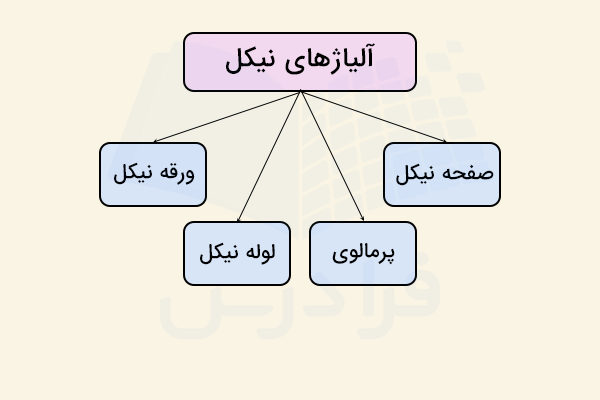
در سمتهای قبل آموختیم نیکل چیست و مهمترین خواص آن کدامند. در ادامه برخی از مهم ترین شکلهای تجاری و آلیاژهای نیکل معرفی شدهاند. این ترکیبات عبارتند از:
- لوله نیکل
- ورقه نیکل
- آلیاژ پرمالوی
- صفحات نیکل
در ادامه یاد می گیریم آلیاژهای رایج عنصر نیکل چیست.
لوله نیکل
لوله نیکل به لوله هایی با قطر کوچک یا بزرگ گفته میشود که از آلیاژهای نیکل تشکیل شدهاند. این لولهها با استفاده از لوله کردن و جوش دادن ورقههای فلزی یا با استفاده از سوراخکاری چرخشی و کشیدن آنها تولید میشود. از این لولهها در بسیاری از صنعت ها، کاربردهای پزشکی و کاربردهای تجاری استفاده میشود. این لولهها در برابر خوردگی، دمای بسیار بالا و فعالیتهای مکانیکی مقاوم هستند.
ورقه نیکل
ورقهای آلیاژی حاوی نیکل در انواع ضخامتها و عرضها موجود هستند و در تمام کاربردهای صنعتی و تجاری قابل استفادهاند. این ورقها با داشتن سطوح مختلف مقاومت در برابر خوردگی، پایداری در دماهای بالا و خواص مکانیکی مناسب، میتوانند جایگزین محصولات لولهای در بسیاری از کاربردها شوند.
این مواد در صنایع شیمیایی، غذایی، داروسازی، انرژی و تولید برق، هوافضا و قطعات هواپیما، استخراج و پالایش نفت و گاز، تجهیزات دریایی، تجهیزات پزشکی و صنعت خودروسازی کاربرد دارند. ورقهای آلیاژی نیکل بر اساس نیازهای خاص تولید میشوند و تمام طیف مواد آلیاژی نیکل را پوشش میدهند.
پرمالوی
پرمالوی، که بیشتر با نام میو – متال ( – متال) شناخته میشود، یک آلیاژ مغناطیسی از نیکل و آهن است و مقادیر کمی از عناصر دیگر مانند مولیبدن و مس نیز در آن وجود دارد. این آلیاژ دارای نفوذپذیری مغناطیسی بسیار بالایی است و به همین دلیل در ساخت محافظهای مغناطیسی بسیار مورد توجه است.

این ورقها در صنایع الکترونیک، مخابرات، تجهیزات علمی و سایر کاربردهای صنعتی که نیاز به کنترل دقیق تعاملات مغناطیسی دارند، استفاده میشوند.
صفحات نیکل
صفحات نیکل خالص و آلیاژی در انواع ضخامتها و عرضها برای تولید قطعات ماشینکاریشده استفاده میشوند. این مواد دارای مقاومت خوب تا عالی در برابر خوردگی، سطوح متنوع تحمل دمایی و ویژگیهای مکانیکی دیگری مانند استحکام، سختی و شکلپذیری هستند.

این صفحات بسیاری از صنایع مانند صنایع شیمیایی، غذایی، داروسازی، انرژی و تولید برق، قطعات و سازههای هوافضا و موشکی، تجهیزات و پالایشگاههای نفتی، محصولات دریایی، سیستمهای پزشکی، تجهیزات صنعتی، کالاهای مصرفی و کاربردهای موتورهای احتراق داخلی کاربرد دارند.
پیشنهاد میکنیم برای درک بهتر روش تولید این تجهیزات و ویژگیهای آنها، فیلم آموزش آبکاری نیکل فرادرس که لینک آن در ادامه آورده شده است را مشاهده کنید.
واکنشهای نیکل
نیکل در دمای اتاق تقریبا واکنش ناپذیر است. این فلز در دمای اتاق با اکسیژن، آب و بسیاری از اسیدها واکنش نمیدهد. به همین دلیل است که در برابر خوردگی مقاوم است. در ادامه توضیح میدهیم واکنشهای شیمیایی عنصر نیکل چیست.
واکنش نیکل و آب
فلز نیکل در آب در شرایط عادی واکنش برقرار نمیکند و در برابر خوردگی مقاوم است.
واکنش نیکل و هوا
در دمای اتاق، نیکل با هوا واکنش نمیدهد. با این وجود، نیکلی که به خوبی پودر شده و خالص باشد، میتواند با هوا واکنش داده و آتشزا شود. در دماهای بسیار بالا، نیکل با اکسیژن واکنش داده و نیکل (اا) اکسید تولید میکند. واکنش نیکل و اکسیژن به شکل زیر است.
واکنش نیکل و هالوژن ها
واکنش نیکل با هالوژنها آهسته انجام میشود. با این وجود، این فلز میتواند با گاز فلوئور واکنش داده و آن را به مادهای مناسب برای تانکهای نگهداری گاز فلوئور تبدیل کند. این فلز همچنین با هالوژنهای برم، کلر و ید واکنش داده و نیکلهالیدها را تولید میکند. در ادامه معادله واکنش این موارد نوشته شده است.
واکنش نیکل با اسیدها
نیکل میتواند به آرامی در سولفوریک اسید رقیق حل شده و یونهای نیکل (اا)، یونهای سولفات و گاز هیدوژن آزاد کند. این واکنش به شکل زیر انجام میشود.
کاربرد عنصر نیکل
در قسمتهای قبل آموختیم عنصر نیکل چیست و ترکیبات آن کدامند. از فلز نیکل استفادههای بسیاری در صنایع مختلف میشود. کلیدیترین کاربرد عنصر نیکل، تولید سکههای پول است. از این عنصر برای تولید سیمهای فلزی مختلف نیز استفاده میشود.
از سایر کاربردهای عنصر نیکل میتوان به موارد زیر اشاره کرد.
- از عنصر نیکل در گاز توربینها و سوخت موشکها استفاده میشود. این فلز میتواند در دماهای بسیار بالا نیز در برابر خوردگی از خود مقاوت نشان دهد.
- از فلز نیکل در تولید آلیاژهای بسیاری استفاده میشود. این آلیاژها در آبکاری تجهیزات، تولید میخ و لولهها استفاده میشود.
- آلیاژ مونل که که از ترکیب نیکل و مس تولید میشود، ترکیبی بسیار سخت است که میتواند در آب دریا در برابر خوردگی مقاومت کند. بنابراین از آن در تولید شفت پروانه در قایقها و نیروگاههای نمکزدایی استفاده میشود.
- از نیکل در بسیاری از فرآیندهای شیمیایی مهم به عنوان کاتالیزگر استفاده میشود.
- از نیکل در ایمپلنت دندانی به علت سازگاری زیستی آن و مقاومت در برابر پلاکهای دندانی استفاده میشود.
- کاتالیز فرایند هیدروژناسیون روغنهای گیاهی
- تولید شیشههای رنگی با رنگ سبز
در ادامه برخی از مهمترین کاربردهای نیکل را توضیح میدهیم.
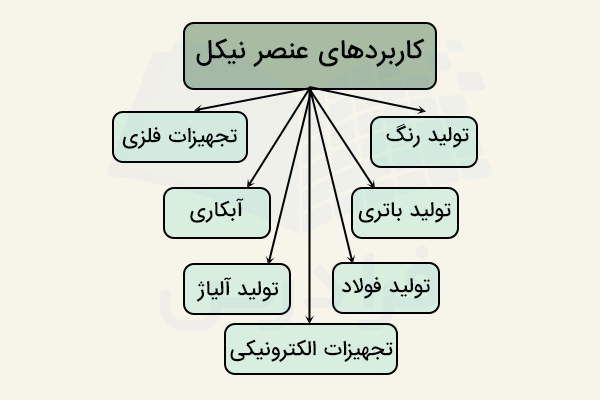
تولید آلیاژ
از آلیاژهای نیکل به خصوص فولاد ضدزنگ در بسیاری از صنایع و وسایل استفاده میشود. برای مثال، فولاد ضدزنگ در بسایری از سازهها، تجهیزات صنعتی، وسایل آشپزخانه و سینک ظرفشویی استفاده میشود. از سایر آلیاژهای نیکل نیز استفادههای بسیار میشود. برای مثال، آلیاژ نیکل و مس به صورت عمده در لولههای استفاده شده برای نمکزدایی آب دریا استفاده میشود.
آبکاری الکتریکی
آبکاری نیز یکی دیگر از کاربردهای عمده فلز نیکل است. آبکاری نیکل برای افزایش مقاومت سطح سایر فلزات در برابر خوردگی استفاده میشود.
تولید تجهیزات فلزی
از صفحات، ورقه و سیم نیکل در تولید بسیاری از وسایل و تجهیزات مانند سنجاقها، بستها و گیرهها، زیورآلات و سیم جراحی استفاده میشود.
تولید فولاد ضد زنگ
از نیکل برای تولید آلیاژ فولاد ضد زنگ استفاده میشود. استفاده از نیکل در این ترکیب باعث افزایش استحکام آن و همچنین مقاومت آن در برابر خوردگی میشود.
خواص مقاوم در برابر خوردگی این فولاد آن را برای ساخت کارد و چنگال، شیرآلات، سینکها، تجهیزات بیرونی، وسایل نقلیه و ظروف آشپزی ایدهآل میکند. فولادهای سازهای با استحکام بالا که نیکل دارند، در صنایع خودرو، هوافضا و ساختوساز کاربرد دارند. تقریبا هر صنعتی که دستگاههای مکانیکی تولید میکند، در مراحل تولید از فولاد ضدزنگ یا سازهای استفاده میکند.
تولید سیم و تجهیزات الکترونیکی
خاصیت چکشخواری و انعطاف نیکل آن را به یک فلز ایده آل برای تولید سیمهای مختلفی تبدیل کرده است که بیشتر در تجهیزات الکتریکی و الکترونیکی استفاده میشود.
باتری نیکل دار
نیکل یکی از مهمترین عناصر استفاده شده در بسیاری از انواع باتری است. برای مثال، باتریهای شارژ شونده نیکل کادمیوم به صورت گستردهای در وسایل الکتریکی و الکترونیکی استفاده میشوند.
تجهیزات روزمره
نیکل در بسیاری از وسایلی که به صورت روزانه با آنها سروکار داریم استفاده میشود. برای مثال، در شارژرها، دوربینهای فیلمبرداری، رادیو اسکنر، سیمهای گیتار، لپتاپ و تلفنهای بیسیم از عنصر نیکل استفاده شده است.
تجهیزات آب شیرین کن
از عنصر نیکل به دلیل مقاومت بالای آن در برابر خوردگی در محیطهای آبی و دریایی و در تجهیزات آب شیرین کن برای نمکزدایی از آب دریا و تبدیل آن به آب شیرین و قابل شرب استفاده میشود.
تولید رنگ
از فلز نیکل در بسیاری از رنگها، محصولات آرایشی و برخی از تجهیزات پلاستیکی به عنوان عامل رنگکننده استفاده میشود. برای مثال، ترکیب نیکل دی متیل گلیوکسیم مادهای است که برای این کار استفاده میشود.
خواص زیستی نیکل
بر اساس تحقیقات انجام شده عنصر نیکل یکی از عناصر حیاتی برای انسانها و جانوران است. با این وجود، کمبود عنصر نیکل در انسانها به وجود نمیآید و استفاده آن به صورت مکمل انجام نمیشود. نیکل مورد نیاز بدن به صورت معمولا با استفاده از مواد غذایی معمول تامین میشود. عمدتا انسانها روزانه مقدار ۱۷۰ میلی گرم نیکل را در رژیم غذایی خود مصرف میکنند.
مقادیر ناچیزی از عنصر نیکل در هوا و محصولات خانگی وجود دارد. این مقادیر به حدی کم هستند که اثری بر سلامت انسان و جانداران ندارند.
مصرف مقادیر زیاد عنصر نیکل میتواند مشکلاتی را برای سلامت انسان به وجود آورد. مقادیر خطرناک مصرف عنصر نیکل چیزی حدود پنجاه هزار تا صدهزار برابر بیشتر از مقدار مصرف روزانه آن است.
خطرات نیکل
بدن انسان مکانیزمهایی برای دفع و جداسازی مقادیر اندک نیکل دارد. فرمهای محلول در آب نیکل که بهصورت ذرات گرد و غبار وارد ریه میشوند، در خون حل میشوند و نیکل همچنین پس از تماس با محصولات حاوی آن میتواند از طریق پوست وارد جریان خون شود. بیشتر نیکل موجود در خون توسط کلیهها دفع شده و از طریق ادرار از بدن خارج میشود. نیکل مصرفشده از دستگاه گوارش عبور میکند اما جذب نمیشود.

مطالعات نشان دادهاند که کارگرانی که در صنایع فلزی در معرض گرد و غبار یا دودهای حاوی نیکل قرار دارند، ممکن است در صورت مواجهه طولانیمدت با ترکیباتی مانند نیکل کربونیل و نیکل سابسولفید، با خطراتی جدی از جمله سرطان مواجه شوند. این یافتهها باعث وضع مقرراتی برای محدود کردن تماس با نیکل در محیط کار شده و بهداشت صنعتی مدرن با کاهش گرد و غبار نیکل و استفاده از تجهیزات حفاظتی، این خطرات را به میزان زیادی کاهش داده است. برای اکثر افراد، مواجهه مزمن با نیکل بسیار نادر است و شایعترین مشکل مربوط به آن، واکنش آلرژیک پوستی است که در ۵ تا ۱۰ درصد افراد رخ میدهد.
حساسیت به نیکل
شایعترین مشکل ناشی از تماس با نیکل، درماتیت تماسی یا التهاب پوستی است که بهدلیل تماس با اشیاء حاوی نیکل مانند سکه، شیرآلات و جواهرات ایجاد میشود. تماس مداوم میتواند باعث حساسیت فرد و واکنش آلرژیک شود، حتی نیکل موجود در غذا نیز ممکن است علائم ایجاد کند. در موارد شدیدتر، حملات آسم گزارش شده است. برای افراد با حساسیت شدید، کاهش مصرف غذایی شامل نیکل توصیه میشود.
نکات ایمنی
برخی اشکال نیکل سرطانزا هستند، اما این اشکال بیشتر در محیطهای صنعتی مانند کارخانههای فرآوری فلزات، پالایش سنگ نیکل و تولید فولاد ضدزنگ یافت میشوند. کارگرانی مانند جوشکاران، آبکاریکنندگان، تولیدکنندگان باتری، جواهرسازان، نقاشان و تولیدکنندگان رنگ و رزین نیز ممکن است در معرض این اشکال نیکل باشند که باید از تجهیزات حفاظتی برای جلوگیری از ورود مقادیر خطرناک نیکل به بدن خود جلوگیری کنند.
مزایای نیکل چیست؟
نیکل مزایای بسیار زیاد و خواص منحصر به فردی دارد که باعث میشود در بسیاری از صنعتها از آن استفاده شود. در ادامه میآموزیم مزایای نیکل چیست.
- مقاومت در برابر خوردگی در محیطهای اسیدی و بازی
- استحکام بالا، پایداری و مقاومت در برابر دماهایی بالا
- هدایت الکتریکی خوب
- خواص مغناطیسی
- سازگاری زیستی
- استفاده در آلیاژهای متنوع
- خاصیت کاتالیستی
- جوشپذیری
معایب نیکل چیست؟
نیکل در کنار خواص ویژهای مانند مقاومت در برابر خوردگی و هدایت الکتریکی و گرمایی بالا، معایبی نیز دارد که ممکن است استفاده از آن را در بسیاری از فرایندها مشکل سازد. برای مثال، این فلز قیمت بالایی داشته و مقادیر زیاد آن برای سلامت انسان مشکلاتی را به وجود میآورد. در ادامه میآموزیم معایب نیکل چیست.
- آلرژی و حساسیت به نیکل از مشکلات رایج این فلز است.
- قیمت بالا
- فرآیندهای خاص و نیازمند افراد حرفهای در تولید برخی از آلیاژها
- محدودیت منابع نیکل و تامینکنندگان آن
- اثرات مخرب زیست محیطی استخراج و پالایش نیکل
- وجود برخی ترکیبات سمی از نیکل
- نیاز به تجهیزات پیشرفته برای تولید اجسام از نیکل به دلیل سختی بالای آن
- ریسک اکسید شدن نیکل در شرایط خاص و دماهای بسیار بالا
- واکنش پذیری نیکل با برخی از مواد خاص
تاریخچه
در این مطلب از مجله فرادرس آموختیم عنصر نیکل چیست و چه کاربردهایی دارد. تاریخچه استفاده از نیکل به ۳۵۰۰ سال قبل از میلاد مسیح برمیگردد که در چین در محصولات آرایشی از آن استفاده میشده است. شناسایی این فلز به عنوان یک عنصر توسط یک دانشمند سوئدی به نام الکس فردریک (Axel Fredrik Cronsted) در سال ۱۷۵۱ میلادی انجام شد که این عنصر را از یک ماده معدنی به نام کوپفرنیکل استخراج کرد.
در قرن ۱۹ میلادی، این فلز در ترکیب با نقره به آلیاژ تبدیل شد. آلیاژ نیکل – نقره ترکیبی بیشتر شبیه به نقره اما سختتر و ارزان قیمتتر است. مقاومت نیکل در برابر خوردگی به استفاده گسترده آن در آبکاری برای مصارف صنعتی مختلف انجامید. استفاده از نیکل در آلیاژ فولاد ضد زنگ در سال ۱۹۱۳ توسط هری بریرلی (Harry Brearley) انجام شد. این کاربرد نیکل باعث تحولی عظیم در صنایع مختلف شد. کاربردهای گسترده نیکل از تزئینات و زیورآلات گرفته تا کاربردهای صنعتی آن، بیانگر اهمیت آن در تمامی صنایع است.
source
