1
مالاریا یک بیماری تهدیدکننده زندگی است که توسط انگلهای Plasmodium ایجاد میشود و از طریق نیش پشههای آلوده منتقل میگردد. این بیماری سالانه تقریباً ۲۵۰ میلیون نفر را در سراسر جهان بیمار میکند و بیش از ۶۰۰,۰۰۰ نفر، عمدتاً کودکان، جان خود را از دست میدهند.
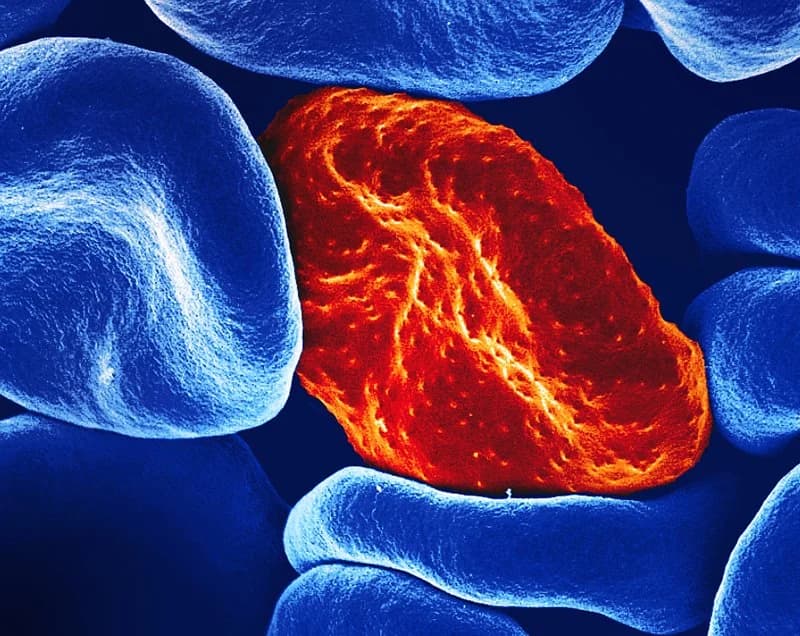
تصویر مرتبط
تصویر بالا یک گلبول قرمز آلوده به انگلهای مالاریا (قرمز) را نشان میدهد. برآمدگیهای کوچک روی سلول آلوده، که به آنها «دکمهها» گفته میشود، به انگل کمک میکنند تا از تخریب شدن جلوگیری کند و التهاب ایجاد کند. سلولهای غیرآلوده (آبی) سطحی صافتر دارند. (منبع: NIAID)
دو واکسن برای کمک به پیشگیری از عفونت مالاریا در کودکان خردسال هماکنون در دسترس هستند. همچنین، آنتیبادیهای مونوکلونال (mAbs) که به انگلهای مالاریا متصل شده و چرخه زندگی آنها را مختل میکنند، توسعه یافتهاند. اما این ابزارها محافظت کاملی در برابر بیماری ایجاد نمیکنند.
واکسنهای مالاریا و آنتیبادیهای مونوکلونالی که تاکنون توسعه یافتهاند، همگی بخش مرکزی پروتئین اصلی به نام PfCSP را که در سطح اسپروزوئیت مالاریا قرار دارد، هدف قرار میدهند. اسپروزوئیتها مرحلهای از زندگی انگل هستند که از طریق پشهها به انسان منتقل میشوند. تا کنون، تحقیقات اهداف دیگری برای پیشگیری از عفونت شناسایی نکرده بود.
کشف یک ناحیه جدید هدف در پروتئین انگل
در یک مطالعه جدید که توسط دکتر جاشوا تان از مؤسسه ملی سلامت آمریکا (NIH) رهبری شد، پژوهشگران نمونههای خونی حدود ۹۵۰ نفر را که قبلاً به مالاریا مبتلا شده بودند، جمعآوری کردند. آنها مجموعهای از آزمایشها را برای جداسازی و شناسایی آنتیبادیهایی که به بخشهایی غیر از ناحیه مرکزی PfCSP متصل میشوند، انجام دادند. نتایج این مطالعه در تاریخ ۳ ژانویه ۲۰۲۵ در نشریه Science منتشر شد.
بیشتر آنتیبادیهایی که به اسپروزوئیتهای موجود در این نمونههای خون متصل شده بودند، همچنین به نسخه آزمایشگاهی PfCSP که به نام rPfCSP شناخته میشود، متصل شدند. اما پس از حذف این آنتیبادیها، در پنج اهداکننده هنوز آنتیبادیهایی وجود داشت که به اسپروزوئیتها متصل میشدند.
پژوهشگران سپس سلولهای B، که مسئول تولید آنتیبادیها هستند، را از این پنج نفر برای بررسی بیشتر غربال کردند. آنها دریافتند که کمتر از ۱٪ سلولهای B مورد مطالعه، آنتیبادیهایی تولید میکردند که به کل اسپروزوئیتها واکنش نشان میدادند اما به rPfCSP متصل نمیشدند. تیم تحقیقاتی ژنهای این سلولهای B را توالییابی کرد و از آنها برای تولید ۱۰ آنتیبادی مونوکلونال جدید استفاده کرد.
شناسایی ناحیه pGlu-CSP
این آنتیبادیهای جدید به پروتئینی در اسپروزوئیتهای زنده متصل شدند که به نظر میرسید PfCSP باشد، اما به نسخه آزمایشگاهی rPfCSP متصل نمیشدند. این یافته نشان میدهد که این آنتیبادیها احتمالاً بخشی از PfCSP را هدف قرار میدهند که در اسپروزوئیتهای زنده تغییراتی دارد. مطالعات بیشتر نشان داد که این آنتیبادیهای جدید به ناحیهای از PfCSP متصل میشوند که تیم تحقیقاتی آن را pGlu-CSP نامگذاری کرد. این ناحیه در rPfCSP آزمایشگاهی قابل دسترس نیست و تنها پس از یک مرحله خاص در رشد اسپروزوئیتهای زنده در معرض قرار میگیرد.
آزمایش آنتیبادی جدید در مدلهای حیوانی
تیم تحقیقاتی قویترین این آنتیبادیها، به نام MAD21-101، را در موشها آزمایش کرد. از میان پنج موشی که قبل از قرار گرفتن در معرض اسپروزوئیتها دوز بالایی از MAD21-101 دریافت کردند، چهار موش تا ۹ روز عاری از عفونت باقی ماندند. در مقابل، موشهایی که این آنتیبادی را دریافت نکرده بودند، سطح بالایی از انگلهای مالاریا را در خون خود داشتند.
بررسی تطابق ژنتیکی انگلهای مالاریا
در مرحله بعد، پژوهشگران توالی ژنی بیش از ۱۶,۰۰۰ انگل مالاریا از سراسر جهان را بررسی کردند. آنها دریافتند که بیشتر این انگلها دارای همان ناحیه pGlu-CSP بودند یا تنها یک جهش منفرد در این ناحیه داشتند که بر اتصال بیشتر آنتیبادیهای جدید، از جمله MAD21-101، تأثیری نداشت.
هیچیک از آنتیبادیهای جدید، از جمله MAD21-101، به توالی PfCSP که در واکسنهای کنونی مالاریا استفاده میشود، متصل نشدند. این موضوع نشان میدهد که درمانهای پیشگیرانه جدید مبتنی بر این آنتیبادیها احتمالاً با استراتژیهای فعلی تداخل نخواهند داشت.
دکتر تان میگوید:
“هنوز کارهای بیشتری باید انجام شود قبل از اینکه این آنتیبادیهای جدید در انسانها آزمایش شوند، اما آنها به عنوان یک افزودنی بالقوه به زرادخانه ضد مالاریای ما امیدبخش هستند.”
source